Гальваническая пара – это процесс взаимодействия двух различных металлов в присутствии электролита, в результате которого возникает разность потенциалов между ними. Данный процесс может приводить к коррозии металлов, особенно в некоторых условиях. Одной из наиболее распространенных гальванических пар является пара алюминия и нержавеющей стали.
Алюминий является активным металлом, а нержавеющая сталь – пассивным металлом. При контакте этих двух металлов в присутствии влаги или электролита, алюминий будет действовать как анод, а нержавеющая сталь – как катод. В результате этого процесса возникнет гальванический ток, который будет вызывать коррозию алюминия.
Коррозия алюминия при гальваническом взаимодействии с нержавеющей сталью может происходить в нескольких формах, включая точечную коррозию, питание и межкристаллитную коррозию. Точечная коррозия проявляется в виде отдельных коррозионных ячеек на поверхности алюминия, питание – в виде отверстий или полостей, а межкристаллитная коррозия затрагивает границы зерен алюминия.
Для предотвращения коррозии алюминия в паре с нержавеющей сталью может быть использована ряд защитных мероприятий. Это может включать применение антикоррозионных покрытий на поверхность алюминия, использование термической обработки для уменьшения чувствительности к коррозии или применение изоляционных материалов между контактирующими поверхностями.
Важность гальванической пары
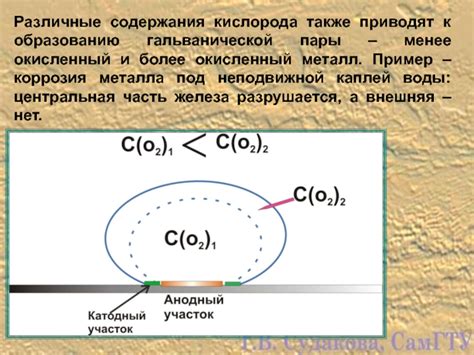
Гальваническая пара алюминия и нержавеющей стали является одним из важных факторов, влияющих на процессы коррозии. Этот феномен основан на разнице в электрохимическом потенциале между разными металлами.
Гальваническая пара возникает, когда два различных металла контактируют между собой в присутствии электролита. В данном случае, алюминий и нержавеющая сталь образуют пару, где алюминий является активным металлом, а нержавеющая сталь - пассивным.
Важность гальванической пары заключается в том, что она может быть причиной различных коррозионных процессов, таких как та плотная атмосфера, высокая влажность, наличие электролита. При возникновении гальванической пары между алюминием и нержавеющей сталью, активный металл (алюминий) становится анодом, а пассивный металл (нержавеющая сталь) - катодом. Это приводит к электрохимическим реакциям, которые способствуют коррозии активного металла.
Поэтому, при проектировании и эксплуатации различных изделий и конструкций из алюминия и нержавеющей стали необходимо учитывать влияние гальванической пары. Особое внимание следует уделять выбору материалов, используемых контактирующих элементов, а также надлежащей изоляции или защите от непосредственного контакта между ними.
Влияние гальванической пары на коррозионные процессы
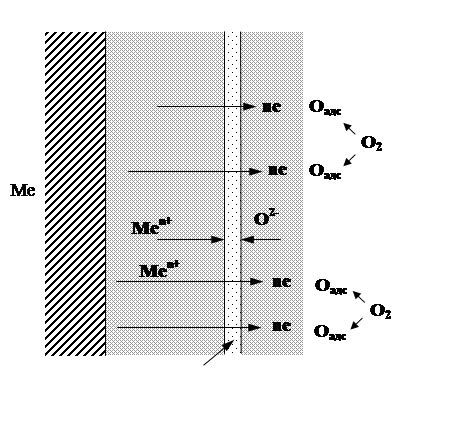
Гальваническая пара, образующаяся при взаимодействии алюминия и нержавеющей стали, может оказывать значительное влияние на коррозионные процессы этих материалов. Гальваническая коррозия - это процесс, при котором один металл становится анодом, а другой - катодом, что приводит к активному растворению анода и образованию коррозионных продуктов.
Алюминий, будучи более активным металлом, становится анодом в гальванической паре с нержавеющей сталью. Это означает, что алюминий будет более подвержен коррозии, а нержавеющая сталь будет охраняться. Такая ситуация может возникать, например, при соединении алюминиевой панели с нержавеющим крепежом на фасаде здания.
Взаимодействие гальванической пары алюминия и нержавеющей стали может вызывать не только активное растворение алюминия, но и изменение химического состава окружающей среды. Коррозионные продукты, образующиеся при взаимодействии анода и катода, могут быть токсичными и негативно влиять на экологическую ситуацию.
Для предотвращения гальванической коррозии и сохранения интегрированной системы, состоящей из алюминия и нержавеющей стали, могут применяться различные меры. Например, использование изоляционных прокладок, специальных покрытий или применение разносортной болтовой или сварной связи может помочь снизить влияние гальванической пары на коррозионные процессы.
Роли алюминия и нержавеющей стали в гальванической паре

Алюминий в гальванической паре с нержавеющей сталью играет роль активного металла. Активность алюминия проявляется в его склонности к электрохимическим окислительно-восстановительным реакциям. При контакте алюминия с нержавеющей сталью возникает электрохимическая ячейка, в которой алюминий выступает в качестве анода. Он окисляется, переходя в ионное состояние, и отдает электроны нержавеющей стали.
Нержавеющая сталь в гальванической паре со своей стороны выступает в качестве пассивного металла. Она обладает высокой устойчивостью к коррозии, особенно благодаря добавлению в состав хрома и никеля. При контакте с алюминием, нержавеющая сталь принимает роль катода. Она принимает электроны, передаваемые алюминием, и происходит восстановительная реакция, предотвращающая окисление стали. Нержавеющая сталь защищает алюминий от коррозии, образуя на своей поверхности защитную пленку оксида.
Роль алюминия и нержавеющей стали в гальванической паре является взаимодополняющей. Алюминий обеспечивает активность системы, выступая в качестве анода и окисляясь, а нержавеющая сталь обладает пассивностью, выступая в качестве катода и предотвращая коррозию образованием защитной пленки. Этот электрохимический процесс защищает оба материала от деструктивного воздействия коррозии и улучшает их долговечность и стабильность в эксплуатации.
Механизмы коррозии
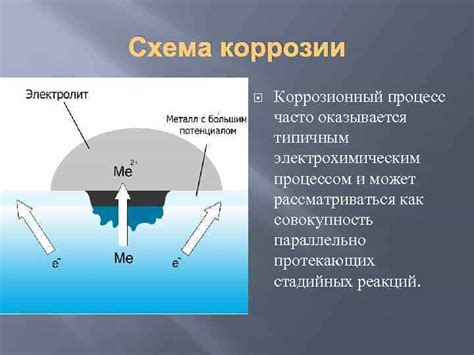
1. Электрохимическая коррозия
Гальваническая пара алюминия и нержавеющей стали приводит к электрохимической коррозии. В данном механизме происходит образование анодных и катодных областей на поверхности металлов, а также передача электронов и ионов от анода к катоду. В результате этого процесса происходит разрушение защитной оксидной пленки на алюминии и образование коррозионных электролитических элементов.
2. Ионная коррозия
Гальваническая пара также способствует появлению ионной коррозии. При этом происходит передача ионов одного металла на поверхность другого, что приводит к разрушению металлической структуры. Ионы могут перемещаться в электролитическом растворе, вызывая образование окислительно-восстановительных реакций и изменение pH среды.
3. Кислородная коррозия
При взаимодействии алюминия и нержавеющей стали возникает кислородная коррозия. Кислород и вода, находящиеся в окружающей среде, попадают на поверхность металлов и вызывают окисление, образование оксидных пленок и дальнейшее разрушение материала. Кислородная коррозия приводит к появлению трещин и пятен на поверхности металлов.
4. Сульфатная коррозия
В случае воздействия сульфатов, находящихся в окружающей среде, на гальваническую пару алюминия и нержавеющей стали возникает сульфатная коррозия. Сульфаты проникают в микротрещины поверхности металлов и вызывают их разрушение. При этом происходит образование серы на поверхности металлов, что приводит к увеличению коррозионных процессов.
Коррозионные процессы алюминия

Алюминий – один из наиболее популярных металлов, который широко используется в различных отраслях промышленности и строительства. Несмотря на высокую стойкость к коррозии, алюминий все же подвержен коррозионным процессам.
Основной причиной коррозии алюминия является его реакция с кислородом воздуха, которая приводит к образованию оксидной пленки на поверхности металла. Однако, эта пленка обладает защитными свойствами и предотвращает дальнейшее продвижение коррозии.
Воздействие различных факторов, таких как влажность, агрессивные среды и механические воздействия, может облегчить разрушение оксидной пленки и создать условия для активной коррозии алюминия.
Особенно высокая коррозионная активность алюминия наблюдается при контакте с металлами с более высокими потенциалами, такими как сталь, что создает условия для возникновения гальванической коррозии. В таком случае, алюминий выступает в роли анода, а сталь – катода, и между ними возникает гальваническая пара.
Гальваническая коррозия алюминия может быть особенно интенсивной в присутствии влаги и электролитов. При этом, проводимость электролита, концентрация растворенных солей и рН среды также оказывают влияние на скорость разрушения алюминиевой поверхности.
Коррозионные процессы нержавеющей стали

Нержавеющая сталь является одним из наиболее распространенных материалов, применяемых в различных отраслях. Однако, она не является полностью устойчивой к коррозии. Коррозионные процессы нержавеющей стали могут происходить под воздействием агрессивной среды, такой как хлориды, сернистый газ или хлориды аммония.
Процесс коррозии нержавеющей стали начинается с образования пассивной пленки на поверхности материала. Эта пленка образуется благодаря наличию хрома в составе стали, который взаимодействует с кислородом и создает защитный слой. Однако, если на поверхность попадают агрессивные вещества или если сталь находится в агрессивной среде продолжительное время, пассивная пленка может разрушиться и начнется процесс активной коррозии.
Активная коррозия нержавеющей стали проявляется в образовании окислов и солей металлов на поверхности материала. Коррозионные процессы могут привести к появлению пятен, пузырьков или кратера на поверхности стали. При этом, сталь может потерять свои механические свойства и прочность, что приводит к снижению ее эксплуатационных характеристик.
Для защиты нержавеющей стали от коррозии используют различные методы. Это может быть нанесение специального покрытия, применение ферритного аустенитного сплава или контроль содержания хрома в стали. Также, можно использовать методы электрохимической защиты, как например, катодная защита или использование гальванических пар.
Вопрос-ответ

Какова основная причина коррозии при контакте алюминия и нержавеющей стали?
Основная причина коррозии при контакте алюминия и нержавеющей стали заключается в возникновении гальванической пары между этими материалами. При наличии электролита (например, влаги) происходит перенос электронов и ионов между анодом (алюминием) и катодом (нержавеющей сталью), что приводит к коррозии алюминия. Нержавеющая сталь, в свою очередь, считается катодом и обычно не подвержена такому роду коррозии.
Какие факторы могут оказывать влияние на интенсивность коррозионных процессов при контакте алюминия и нержавеющей стали?
Интенсивность коррозионных процессов при контакте алюминия и нержавеющей стали может зависеть от нескольких факторов. Важными являются такие параметры, как качество поверхности материалов, наличие и состав электролита, температура окружающей среды, наличие механических напряжений и др. Также влияние на коррозию может оказывать биологическая активность среды, в которой эксплуатируются материалы.
