Йод является химическим элементом с атомным номером 53 и относится к галогенам. Один из наиболее известных его свойств - способность растворяться в некоторых металлах. Растворение йода в различных металлах имеет свои особенности и зависит от химических свойств металла и условий реакции.
Некоторые металлы, такие как железо, алюминий, цинк и магний, проявляют реакцию с йодом и могут растворять его. Однако эта реакция происходит только при наличии определенных условий, например, когда металл находится в порошкообразном состоянии или имеет большую поверхность контакта с йодом.
Йод также может растворяться в кристаллических структурах некоторых металлов, например, в металлах группы переходных элементов. В таких случаях растворение йода происходит благодаря взаимодействию между йодом и атомами металла, которые образуют комплексные соединения.
Некоторые металлы, такие как золото, серебро и платина, не растворяют йод и не проявляют с ним реакцию. Это связано с их химической стабильностью и низкой активностью в химических реакциях.
Изучаем, как йод растворяет разные металлы

Йод – химический элемент из группы галогенов, который может растворяться в различных металлах. Растворение йода в металлах происходит благодаря химическим реакциям между ионами йода и металлическими ионами.
Реакция между йодом и металлами может приводить к образованию соединений, таких как йодиды. Йодиды могут быть растворимыми или нерастворимыми в воде, и это влияет на скорость реакции и процесс растворения йода в металлах.
Обычно йод растворяется в металлах, таких как алюминий, железо, цинк, медь и свинец. Однако скорость растворения и эффективность этого процесса могут различаться в зависимости от конкретного металла и условий реакции.
Важно отметить, что растворение йода в металлах может быть не обратимым процессом, что означает, что однажды растворившись, йод не может быть легко удален из металла. Это может быть полезным свойством в некоторых промышленных процессах, но также может создавать проблемы при попытке удалить или очистить металл, содержащий йод.
Исследования в области растворения йода в металлах продолжаются, и специалисты постоянно ищут новые способы и приложения этого процесса. Знание о том, как йод растворяет различные металлы, может быть полезно при разработке новых материалов или технологий.
Свойства йода и его реакция с металлами

Йод - это химический элемент, который принадлежит к галогенам. Он обладает характерным фиолетовым цветом и может образовывать пары при комнатной температуре, что делает его видимым голым глазом. Йод является хорошим окислителем и может реагировать с разными веществами, включая металлы.
Йод обычно растворяется в некоторых металлах, таких как алюминий, цинк и железо. При реакции йод окисляется, а металлы восстанавливаются. Эта реакция происходит при нагревании металла с йодом или при образовании смеси измельченного металла и йода, которая затем нагревается.
При реакции йод медленно окисляется кислородом и образует соединения с металлами, такими как йодиды. Например, металлический цинк растворяется в йоде, образуя желтый йодид цинка. Алюминий также может реагировать с йодом, образуя алюминиевый йодид.
Реакция между йодом и металлами может происходить при комнатной температуре, но обычно она протекает быстрее при нагревании. Металлы могут растворяться в йоде с образованием йодидов, которые могут иметь различные цвета, в зависимости от металла.
Реакция йода и металлов является достаточно изученной и имеет применение в различных процессах, включая производство сплавов и других химических соединений.
Влияние электронной структуры металла на его растворимость в йоде
Растворимость металлов в йоде зависит от их электронной структуры, которая определяет химические свойства и взаимодействие с другими веществами. Электронная структура металлов характеризуется количеством электронов во внешнем энергетическом уровне, а также их распределением по подуровням.
Имеются несколько факторов, которые влияют на растворимость металлов в йоде. Один из них - это электронное состояние металла. Металлы с полностью заполненными или полностью опустошенными внешними энергетическими уровнями обычно малорастворимы в йоде.
Однако, металлы с не полностью заполненными внешними энергетическими уровнями могут образовывать стабильные соединения с йодом. Например, алюминий (Al) имеет электронную конфигурацию 2, 8, 3, где 3 электрона на внешнем энергетическом уровне, поэтому он способен реагировать с йодом.
Кроме того, растворимость металлов в йоде также может быть связана с их электрохимическим потенциалом. Металлы с более высоким электрохимическим потенциалом обычно легче растворяются в йоде, так как они обладают большей химической активностью и большими возможностями для электронного переноса.
Таким образом, электронная структура металла играет важную роль в его растворимости в йоде. Она определяет способность металла образовывать стабильные соединения с йодом и его реакционную активность в данной системе. Изучение этих взаимосвязей позволяет лучше понять химические свойства и взаимодействие металлов с другими веществами.
Растворимость щелочных металлов в йоде
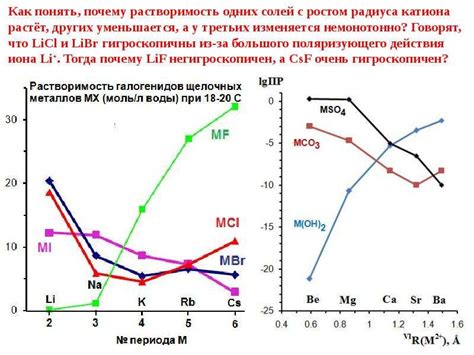
Йод является одним из самых химически активных и агрессивных элементов, способных растворять в себе различные металлы. Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, также могут быть растворены в йоде.
Взаимодействие между йодом и щелочными металлами основано на образовании йодидов металлов. При этом происходит окислительно-восстановительная реакция, в результате которой щелочные металлы окисляются, а йод восстанавливается.
Растворимость щелочных металлов в йоде зависит от множества факторов, включая температуру, концентрацию йода, размер и структуру металлической поверхности, а также время взаимодействия.
При взаимодействии щелочных металлов с йодом происходит выделение водорода и образование йодидных иодатных солей. Растворимость этих солей может быть повышена путем добавления катализаторов или повышения температуры. Однако, во избежание осложнений, такие реакции следует проводить с осторожностью и под контролем специалистов.
Реакция йода с щелочноземельными металлами

Йод — химический элемент, который взаимодействует с различными металлами, включая щелочноземельные металлы. Реакция йода с этими металлами происходит при нагревании, и результатом этой реакции является образование соответствующих металлических йодидов.
Например, реакция йода с магнием приводит к образованию магниевого йодида (MgI2), который представляет собой белый кристаллический порошок. Этот соединение обладает высокой стабильностью и хорошо растворим в водных растворах.
Аналогично, йод взаимодействует с кальцием, образуя кальциевый йодид (CaI2). Этот соединение также является белым кристаллическим порошком, который отличается высокой стабильностью и растворимостью в воде.
Следует отметить, что реактивность йода с щелочноземельными металлами возрастает с увеличением атомного номера металла. Например, барий, которому соответствует атомный номер 56, реагирует с йодом с большей интенсивностью, чем кальций, атомный номер которого равен 20.
Таким образом, реакция йода с щелочноземельными металлами приводит к образованию соответствующих металлических йодидов, которые характеризуются высокой стабильностью и растворимостью в воде.
Взаимодействие йода с прочими железами
Йод – химический элемент, который проявляет активность при контакте с различными металлами. Однако, не все металлы могут быть растворены в йоде. Растворение металла в йоде возможно при образовании комплексных соединений или химических реакциях, которые приводят к образованию йодидных иодных солей.
Один из наиболее известных примеров взаимодействия металла с йодом – реакция растворения железа. Железо может реагировать с йодом и образовывать йодид железа. При этом образующийся йодид железа имеет голубовато-зеленый цвет и является растворимым в воде.
Другим примером взаимодействия йода с металлами является растворение меди. При контакте йода с медью происходит образование йодида меди. Йодид меди имеет черный цвет и также растворим в воде. Эта реакция может происходить при нагревании.
Однако, не все металлы могут растворяться в йоде. Например, алюминий, цинк и свинец не растворяются в йодном растворе. Они остаются неподвижными и не образуют йодидов.
Явления растворения металлов в йоде имеют большое значение как в химии, так и в промышленности. Поэтому, изучение взаимодействия йода с прочими железами является важной задачей для химической науки.
Сравнение растворимости йода с различными металлами
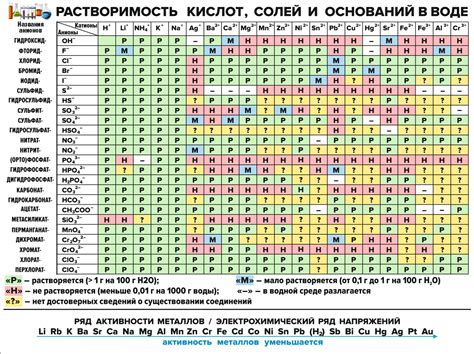
Йод - это элементарный химический элемент, который образует соединения с различными веществами, включая металлы. Растворимость йода в металлах зависит от их химических свойств и структуры.
Серебро является одним из металлов, с которыми йод образует соединения. Йод легко растворяется в серебре при нагревании, образуя йодид серебра, который имеет желтоватый оттенок. Йодид серебра обладает высокой устойчивостью и используется в фотографии для создания пленки.
Медь также образует соединения с йодом. Растворимость йода в меди зависит от его структуры и способности связывать себя с йодом. В зависимости от условий реакции, образующийся йодид меди может иметь различные цвета - от белого до желтого.
Цинк реагирует с йодом, образуя йодид цинка. Растворимость йода в цинке зависит от его поверхности и структуры. Цинк вступает в реакцию с йодом, в результате чего образуется белый йодид цинка.
Железо также может растворять йод. Растворимость йода в железе зависит от его структуры и состава. Железо может образовывать различные йодиды, включая бесцветные или желтоватые соединения.
Алюминий реагирует с йодом, образуя йодид алюминия. Растворимость йода в алюминии зависит от различных факторов, включая концентрацию йода и температуру реакции. Йодид алюминия может иметь различные цвета, в зависимости от условий реакции.
В целом, растворимость йода с различными металлами может быть различной и зависит от их химической структуры и свойств. Изучение растворимости йода с различными металлами является важной темой для развития металлургической и химической промышленности.
Вопрос-ответ

Какие металлы растворяет йод?
Йод может растворяться в разных металлах, включая алюминий, цинк и свинец. Однако наиболее известными металлами, с которыми йод реагирует, являются железо и медь.
Как йод взаимодействует с металлами?
Когда йод взаимодействует с металлами, происходит окислительно-восстановительная реакция. йод окисляется до йодида, а металл восстанавливается. Например, железо окисляется до йодида железа, который имеет синий цвет.
Могут ли все металлы растворять йод?
Нет, не все металлы могут растворять йод. Йод способен растворяться только в определенных металлах, которые обладают достаточной активностью для взаимодействия с йодом.
Какие свойства должны быть у металлов, чтобы они растворяли йод?
Для того чтобы металл мог растворять йод, он должен обладать достаточной активностью и способностью вступать в окислительно-восстановительные реакции. Такие металлы, как железо и медь, соответствуют этим требованиям и могут растворять йод.
Какие еще вещества могут растворять йод?
Вещества, способные растворять йод, включают также некоторые органические соединения, например, этанол (спирт), ацетон и гексан. Эти соединения могут служить хорошим растворителем для йода.
