Химическая реакция железа с разбавленными растворами серной кислоты является одной из наиболее распространенных и важных в химии. Эта реакция является примером окислительно-восстановительной реакции, где железо выступает в качестве восстановителя и серная кислота – в качестве окислителя.
При взаимодействии железа с разбавленными растворами серной кислоты образуются соли сульфата железа и выделяется водород. Данная реакция сопровождается эволюцией газа, что можно заметить по появлению пузырьков газа в растворе и по характеристическому шипению. Такая реакция является стандартной лабораторной процедурой по получению водорода.
Кроме того, реакция железа с разбавленными растворами серной кислоты может использоваться в качестве метода для определения концентрации кислоты в растворе. По объему образовавшегося водорода можно рассчитать количество кислоты, приняв во внимание стехиометрию реакции.
Взаимодействие железа с разбавленными растворами серной кислоты: основные этапы
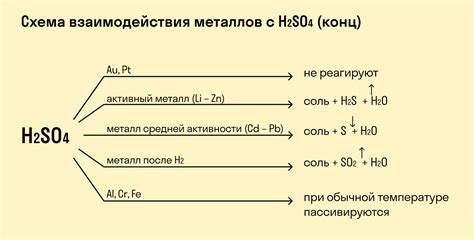
Этап 1: Образование ионов железа
При взаимодействии железа с разбавленными растворами серной кислоты происходит окислительно-восстановительная реакция. Серная кислота вступает в реакцию с металлическим железом, образуя ионы железа Fe(II) и серульяционнокислоту H2SO4. Этот процесс сопровождается выделением газов.
Этап 2: Формирование отложений
Ионы железа Fe(II) продолжают реагировать с серной кислотой, превращаясь в ионы железа Fe(III). После этого они соединяются с отдельными атомами серы и формируются сложные соединения железа и серы, так называемые гидросульфаты железа. Эти соединения образуют характерные осадки, нерастворимые в воде.
Этап 3: Протекание реакции
Протекание реакции зависит от концентрации серной кислоты в растворе и от температуры. При небольшой концентрации кислоты реакция происходит медленно, а при повышенной концентрации – более интенсивно. Также высокие температуры способствуют более быстрому протеканию реакции.
Этап 4: Реакция газового выделения
В процессе взаимодействия железа с разбавленными растворами серной кислоты выделяется газ – водород (H2). Выделение газа становится заметным на ранних стадиях реакции и становится более интенсивным во время образования ионов железа и гидросульфатов.
Реактивность железа в разбавленных растворах серной кислоты
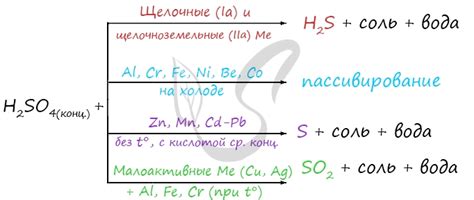
Железо является химическим элементом, который может проявлять высокую реактивность при взаимодействии с разбавленными растворами серной кислоты. Данная реакция основана на образовании сульфата железа и выделении водорода.
В процессе взаимодействия железа с разбавленной серной кислотой происходит окислительно-восстановительная реакция. В результате этой реакции железо окисляется до ионов двухвалентного состояния (Fe2+), а серная кислота восстанавливается до сернистой кислоты (H2SO3).
Реактивность железа в разбавленных растворах серной кислоты зависит от концентрации и температуры раствора. При повышении концентрации и температуры раствора, реакция происходит более интенсивно.
Однако следует учитывать, что взаимодействие железа с концентрированными растворами серной кислоты может привести к образованию опасных химических соединений. Поэтому при работе с такими растворами необходимо соблюдать меры безопасности и проводить эксперименты лишь в специально оборудованных лабораториях.
Химические реакции при взаимодействии железа с разбавленными растворами серной кислоты

Железо, являясь одним из самых распространенных металлов, вступает во взаимодействие с различными химическими соединениями. При взаимодействии с разбавленными растворами серной кислоты происходят интересные химические реакции, которые можно использовать в различных областях науки и техники.
Основной химической реакцией, происходящей при взаимодействии железа с серной кислотой, является образование водорода. При этом железо реагирует с серной кислотой, образуя сульфат железа(II) и выделяя молекулы водорода. Реакция происходит с выделением тепла и обычно сопровождается шипением. Реакция представляет собой окислительно-восстановительную реакцию, где железо окисляется, а водород восстанавливается.
Образовавшийся водород может быть использован в различных промышленных и научных процессах. Например, водород может быть использован в качестве топлива в бреннерах для получения высоких температур или в водородных пушках для создания высоконапорных струй. Кроме того, окислительные свойства серной кислоты позволяют использовать ее в процессе получения железосодержащих соединений, таких как сернокислое железо(II), которые находят широкое применение в медицине, химической промышленности и других отраслях.
В общем, взаимодействие железа с разбавленными растворами серной кислоты является одной из важных химических реакций, позволяющей получить водород и различные железосодержащие соединения. Эти реакции имеют широкое применение в различных областях науки и техники и продолжают быть предметом исследований и разработок.
Влияние концентрации серной кислоты на скорость реакции с железом

Реакция между железом и разбавленной серной кислотой является одной из основных химических реакций, происходящих в промышленности. Исследование влияния концентрации серной кислоты на скорость данной реакции представляет большой интерес для практического применения.
Эксперименты показывают, что изменение концентрации серной кислоты влияет на скорость реакции с железом. При повышении концентрации кислоты, скорость реакции также увеличивается. Это обусловлено тем, что большее количество ионов водорода в растворе серной кислоты способствует активации атомов железа и ускорению химической реакции.
Однако, также важно отметить, что с увеличением концентрации серной кислоты, реакция может протекать более интенсивно, что может привести к повышению температуры среды и неконтролируемых химических процессов. Поэтому при проведении данной реакции необходимо тщательно контролировать концентрацию кислоты.
Вместе с тем, наблюдается насыщение скорости реакции с увеличением концентрации серной кислоты. Увеличение концентрации после определенного значения не приводит к дальнейшему увеличению скорости реакции. Это может быть связано с насыщением активных центров раствора железом или другими причинами, требующими дальнейшего исследования.
Применение взаимодействия железа с разбавленными растворами серной кислоты
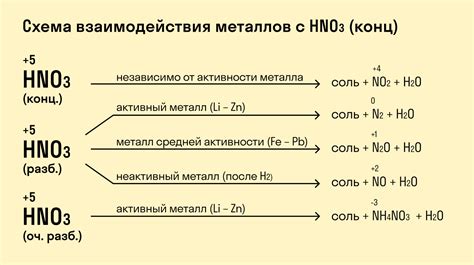
Взаимодействие железа с разбавленными растворами серной кислоты находит применение в различных областях науки и промышленности. Оно является важным этапом промышленных процессов, таких как добыча металлов, производство щелочей, удобрений и других химических веществ. Образующиеся продукты реакции могут использоваться во множестве сфер, начиная от пищевой промышленности и заканчивая медицинскими исследованиями.
Одним из основных применений реакции железа с разбавленными растворами серной кислоты является получение железосодержащих соединений. Эти соединения широко используются в производстве органических и неорганических веществ, например, в качестве катализаторов и красителей. Кроме того, они применяются в технологиях очистки воды и воздуха, в процессах синтеза новых материалов и в других областях химической промышленности.
Реакция железа с разбавленными растворами серной кислоты также играет важную роль в аналитической химии. Этот метод используется для определения концентрации железа в образцах различного происхождения. Благодаря этому, ученые и аналитики могут проводить анализы и исследования, связанные с металлами и окружающей средой, такие как изучение загрязнения водных ресурсов или контроль качества пищевых продуктов.
В целом, взаимодействие железа с разбавленными растворами серной кислоты имеет широкие применения и является важным компонентом химической промышленности и научных исследований. Это позволяет получать различные продукты, используемые в разных отраслях исследований и производства, а также проводить анализы и контроль качества.
Вопрос-ответ

Что происходит при реакции железа с разбавленными растворами серной кислоты?
При реакции железа с разбавленными растворами серной кислоты происходит образование сульфата железа(II) и выделение водорода.
Каковы основные свойства реакции железа с разбавленными растворами серной кислоты?
Основными свойствами реакции железа с разбавленными растворами серной кислоты являются образование сульфата железа(II) и выделение водорода. При этом, железо обладает свойством растворяться в серной кислоте и образовывать ион железа(II), который затем соединяется с ионами серной кислоты.
Как выполняется реакция железа с разбавленными растворами серной кислоты в лаборатории?
Для выполнения реакции железа с разбавленными растворами серной кислоты в лаборатории необходимо взять небольшой кусочек железа и поместить его в колбу с разбавленной серной кислотой. При этом образуется сульфат железа(II), а из колбы выделяется газовая фаза, включающая водород.
Какие еще реакции могут происходить при взаимодействии железа с разбавленными растворами серной кислоты?
При взаимодействии железа с разбавленными растворами серной кислоты также может происходить реакция образования гидроксосульфата железа(II) и образование сульфата железа(III). Эти реакции происходят в зависимости от условий проведения эксперимента.
