В химии 9 класса одной из важных тем является положение металлов в периодической системе. Понимание этой темы поможет учащимся лучше понять и объяснить свойства металлов и использовать их в практических задачах.
Положение металлов в периодической системе химических элементов определяется их атомным строением и свойствами. Металлы обладают такими характеристическими свойствами, как высокая тепло- и электропроводность, блеск, способность образовывать ионы с положительным зарядом. Они обычно находятся слева от линии, разделяющей металлы и неметаллы в периодической системе.
Положение металлов в периодической системе сильно влияет на их свойства и способность образовывать соединения. Металлы, находящиеся выше в периодической системе, обычно имеют более активные свойства и более легко образуют соединения с неметаллами. Однако, снижение активности металлов происходит при движении вниз по группе.
Важно отметить, что положение металлов в периодической системе также влияет на их способность проявлять кислотные и основные свойства. Металлы слева в периодической системе обычно проявляют основные свойства, тогда как металлы справа имеют склонность проявлять кислотные свойства.
В конспекте по химии 9 класса рассматривается подробная классификация металлов, их основные свойства и способы получения. Изучение положения металлов в периодической системе поможет учащимся лучше понять и запомнить свойства их соединений и использовать этот материал в дальнейшем изучении химии.
Основные понятия по химии 9 класс: положение металлов
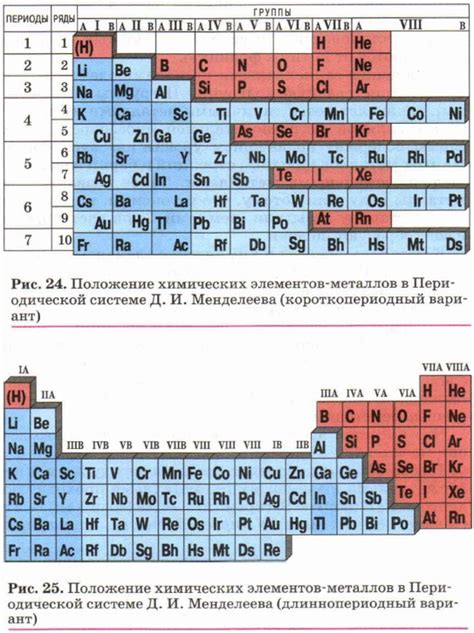
Положение металлов в периодической системе химических элементов имеет важное значение в изучении химии. Металлы - это элементы, обладающие такими химическими свойствами, как проводимость электричества и тепла, гладкое блеск и способность образовывать соединения с кислородом.
Периодическая система химических элементов представляет собой таблицу, в которой элементы располагаются в порядке возрастания атомного номера. Основные блоки периодической системы можно разделить на металлы, неметаллы и полуметаллы.
Металлы охватывают большую часть периодической системы. Они расположены слева и снизу таблицы. Металлы характеризуются высокой электропроводностью и теплопроводностью. Они также способны легко давать электроны и образовывать положительные ионы.
Металлы могут быть разделены на активные и пассивные в зависимости от их способности реагировать с другими веществами. Активные металлы реагируют с кислородом, водой и кислотами, образуя соединения. Пассивные металлы, напротив, обладают химической инертностью и реакции происходят очень медленно.
- Активные металлы включают натрий, калий, кальций и многое другое.
- Пассивные металлы включают золото, серебро, платину и другие драгоценные металлы.
Некоторые металлы также обладают способностью создавать сплавы с другими металлами. Сплавы - это смеси металлов, обладающие новыми свойствами и применяемые в различных отраслях промышленности.
| Тип металла | Примеры |
|---|---|
| Активные металлы | Натрий, калий, кальций и др. |
| Пассивные металлы | Золото, серебро, платина и др. |
Знание о положении металлов в периодической системе позволяет нам лучше понять их свойства и использовать их в различных областях науки и промышленности.
Положение металлов в периодической системе Менделеева

Положение металлов в периодической системе Менделеева определяется их химическими и физическими свойствами. Металлы занимают большую часть периодической системы и находятся слева от линии, разделяющей металлы и неметаллы.
Одним из основных химических свойств металлов является способность образовывать положительные ионы, отдавая электроны. Это связано с тем, что внешний электронный слой атома металла содержит малое количество электронов, что обуславливает их легкость отдачи электронов при реакциях. Эта способность объясняет металлический блеск и характерные свойства металлов, такие как хорошая тепло- и электропроводность, пластичность и прочность.
В периодической системе Менделеева металлы разделены на несколько групп. Первая группа состоит из щелочных металлов, таких как литий, натрий, калий. Они имеют низкую плотность, низкую температуру плавления и кипения, а также являются очень реактивными и взрывоопасными.
Вторая группа состоит из щёлочноземельных металлов, например, магний, кальций, стронций. Они также реактивны, но менее, чем щелочные металлы, и обладают более высокой плотностью и температурой плавления и кипения.
Другая группа металлов - переходные металлы, которые занимают особое положение в периодической системе. Они имеют высокую плотность, более сложные электронные оболочки и способность образовывать ионы с разными валентностями. Переходные металлы включают в себя такие элементы, как железо, медь, цинк.
Химические свойства металлов
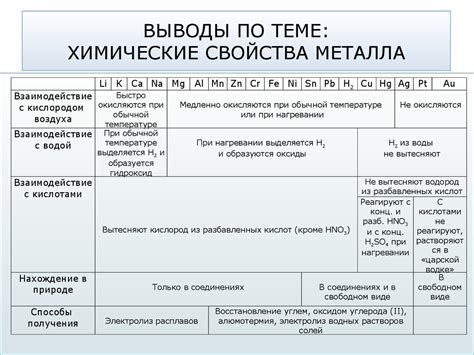
Химические свойства металлов определяются их способностью образовывать ионы положительного заряда, способностью вступать в реакции с другими веществами и образовывать соединения.
Одной из основных химических свойств металлов является их способность реагировать с кислородом, образуя оксиды. Оксиды, образующиеся при реакции металлов с кислородом, могут быть щелочными, амфотерными или кислыми.
Металлы также обладают способностью вступать в реакции с кислотами, при этом выделяется водород. Реакция металла с кислотой протекает с образованием соответствующей соли и выделением водорода.
Металлы могут быть восстановлены из солей при взаимодействии с водородом, электрическим током или другими веществами. Восстановление металлов происходит за счет передачи электронов.
Свойства металлов также проявляются при реакциях с водой. Некоторые металлы реагируют с водой, образуя основания и выделяя водород, другие металлы (например, железо) реагируют только с паром воды или водяным раствором кислоты.
Использование металлов в промышленности и повседневной жизни

Металлы имеют широкое применение в промышленности и повседневной жизни благодаря своим уникальным свойствам. Они обладают высокой прочностью, теплопроводностью, электропроводностью и устойчивостью к коррозии.
В промышленности металлы используются в производстве различных изделий. Например, железо и сталь являются основными материалами для строительства мостов, зданий, машин и транспорта. Алюминий используется для производства авиационных и автомобильных деталей, а также упаковочных материалов.
Медь широко используется в электротехнике, так как она является хорошим проводником электричества. Она применяется при производстве электропроводки, электронных компонентов и проводов. Также медь используется для производства монет, украшений и кухонной посуды.
Цинк и олово обладают свойством покрываться пленкой оксида, что защищает изделия из них от коррозии. Это свойство используется при производстве металлических конструкций, автомобильных кузовов и холодильников.
Серебро и золото широко применяются в ювелирной и часовой промышленности. Они используются для производства украшений, часовых механизмов и предметов роскоши. Кроме того, золото применяется в медицине для изготовления стоматологических пломб и протезов.
В повседневной жизни металлы также находят применение. Многие предметы, которыми мы пользуемся каждый день, содержат металлы. Например, посуда из нержавеющей стали, столовые приборы из серебра, металлические зажигалки и карандаши.
Таким образом, металлы играют важную роль в промышленности и повседневной жизни людей, обеспечивая прочность и функциональность различных изделий и материалов. Их уникальные свойства делают их необходимыми для многих процессов и применений.
Вопрос-ответ

Какие металлы рассматриваются в 9 классе?
В 9 классе рассматриваются такие металлы, как железо, цинк, алюминий, медь, свинец, а также их соединения.
Каково положение металлов в периодической системе?
Металлы в периодической системе расположены слева от ступени бора и с понижением от легких к тяжелым металлам.
Как влияет положение металла в периодической системе на его реакционную способность?
Чем левее и выше металл расположен в периодической системе, тем более активным он является и тем сильнее его способность к реакциям с кислородом, водой и кислотами.
Какие свойства металлов определяются их положением в периодической системе?
Положение металлов в периодической системе определяет их атомное строение, электроотрицательность, размеры атомов, заряд ядра и другие факторы, которые в свою очередь влияют на их химические и физические свойства.
