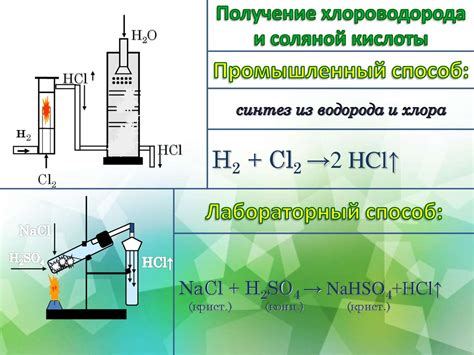
Кислота хлороводородная (HCl) является одной из наиболее распространенных и изученных кислот. Она обладает химическими свойствами, позволяющими взаимодействовать с различными веществами, в том числе с металлами. В данной статье мы рассмотрим основные реакции и свойства этого взаимодействия.
Когда кислота HCl встречает металл, происходит реакция окисления металла и одновременное восстановление водорода. При этом выделяется большое количество теплоты и продуктами реакции являются хлорид металла и водород. Реакция HCl с металлами происходит достаточно быстро и сопровождается выделением пузырей газа и характерным звуком.
При взаимодействии кислоты HCl с металлами образуется соответствующий хлорид металла. Некоторые металлы, такие как калий (K), натрий (Na), кальций (Ca) и алюминий (Al), активно реагируют с HCl и протекают сильно теплореактивные реакции. Другие металлы, такие как медь (Cu), серебро (Ag) и золото (Au), реагируют нестабильно с кислотой и образуют менее активные хлориды.
Влияние HCl на металлы

Кислота хлористоводородная (HCl) обладает выраженным влиянием на металлы, вызывая различные реакции и свойства. Взаимодействие HCl с металлами может протекать с образованием солей и выделением водорода, а также сопровождаться коррозией и растворением металлической поверхности.
Одной из основных реакций взаимодействия HCl с металлами является выделение водорода. При этом металл реагирует с кислотой, образуя соль металла и газовый водород. Реакция может протекать с разной интенсивностью в зависимости от металла и концентрации кислоты. Например, активные металлы, такие как натрий или калий, реагируют с HCl быстро и горячо, выделяя значительное количество водорода.
Кроме того, HCl проявляет свойства коррозии по отношению к некоторым металлам. Гидроксид хлорида металла, образующийся в результате реакции, обычно является плохорастворимым и осаждается на поверхности металла, образуя пленку, которая может защищать металл от дальнейшей коррозии.
В некоторых случаях HCl может растворять металлы с образованием хлоридов металла. Например, реакция между HCl и алюминием протекает с образованием хлорида алюминия и выделением водорода. Также данная реакция может быть использована для очистки поверхности алюминиевых изделий от оксида алюминия.
Важность реакции между HCl и металлами

Реакция между соляной кислотой (HCl) и металлами является одной из основных реакций, которые происходят в химических процессах. Эта реакция имеет большое значение и применяется в различных областях науки и технологии. Взаимодействие HCl с металлами происходит с образованием солей и выделением водорода.
Во-первых, реакция HCl с металлами является одним из методов получения солей. При взаимодействии соляной кислоты с металлом образуется хлорид металла и выделяется водород. Полученные хлориды широко применяются в различных отраслях промышленности, например, в производстве удобрений, стекла и пластмасс, а также в медицине и лабораториях.
Во-вторых, реакция HCl с металлами позволяет изучать и определять свойства и характеристики металлов. Это является важным в химическом анализе и исследованиях различных материалов. Особенности реакции между HCl и металлом могут дать информацию о его активности, электрохимических свойствах и степени взаимодействия с другими веществами.
Кроме того, реакция HCl с металлами имеет применение в химической промышленности и технологии. Например, эта реакция используется при очистке и удалении окислов и других загрязнений с металлических поверхностей перед их дальнейшей обработкой и использованием. Также реакция HCl с металлами может быть использована для регенерации и восстановления различных каталитических систем и их компонентов.
Таким образом, реакция HCl с металлами является важной и полезной для различных областей науки и производства. Она позволяет получать соли, изучать свойства металлов и применять их в различных технологических процессах.
Химическая реакция между HCl и металлом

Химическая реакция между хлоридом водорода (HCl) и металлом зависит от свойств конкретного металла. HCl, являясь сильной кислотой, проявляет активность при взаимодействии с многими металлами. Реакция происходит за счет образования соли и выделения водорода.
Металлы, которые активно реагируют с HCl, включают такие элементы, как цинк, железо, медь, свинец и алюминий. При контакте с ними, хлорид водорода окисляет металл, выделяя молекулы водорода в газообразном состоянии. Эта реакция сопровождается образованием хлоридов металла.
Например, при взаимодействии цинка с HCl образуется хлорид цинка (ZnCl2) и выделяется водород:
- 2HCl + Zn → ZnCl2 + H2
Подобные реакции можно наблюдать с другими металлами, такими как железо, медь и алюминий. Однако, конкретные условия взаимодействия (концентрация HCl, температура, наличие катализаторов) могут влиять на интенсивность реакции и скорость образования продуктов.
Интересно отметить, что некоторые металлы, такие как золото, платина и серебро, не реагируют с HCl. Это связано с их химической инертностью и высокой устойчивостью к воздействию кислот.
Основные реакции между HCl и металлами

1. Реакция между хлороводородной кислотой и активными металлами:
Активные металлы, такие как натрий (Na), калий (K), литий (Li) и магний (Mg), реагируют с хлоридом водорода (HCl) с образованием соли металла и выделением водорода (H2). Например, реакция между натрием и HCl будет выглядеть следующим образом:
2Na + 2HCl → 2NaCl + H2
2. Реакция между хлороводородной кислотой и менее активными металлами:
Менее активные металлы, такие как алюминий (Al), цинк (Zn) или железо (Fe), также реагируют с HCl, но с разными реакционными характеристиками. Например, алюминий реагирует с HCl, но реакция сопровождается выделением водорода и образованием соли:
2Al + 6HCl → 2AlCl3 + 3H2
3. Реакция между хлороводородной кислотой и недорогими металлами:
Некоторые недорогие металлы, такие как свинец (Pb) и олово (Sn), также могут реагировать с HCl. В данном случае образуется соль металла и выделяется водород. Например:
Pb + 2HCl → PbCl2 + H2
4. Реакция между хлороводородной кислотой и редкоземельными металлами:
Редкоземельные металлы, такие как церий (Ce) или празеодим (Pr), также могут реагировать с HCl. В данном случае образуется хлорид металла и выделяется водород. Например:
2Ce + 6HCl → 2CeCl3 + 3H2
Таким образом, реакция между HCl и металлами может приводить к образованию различных хлоридов металлов и выделению водорода в зависимости от природы и активности металла.
Свойства реакции HCl с металлами

1. Образование солей: При взаимодействии с металлами, хлороводород образует соли, которые являются основным продуктом реакции. Например, реакция хлороводорода с натрием приводит к образованию хлорида натрия (NaCl).
2. Выделение водорода: Реакция хлороводорода с металлами протекает с выделением водорода. Это связано с тем, что хлороводород – это соединение водорода с хлором, и при взаимодействии его с металлом происходит замещение водорода в молекуле хлороводорода на металл. Таким образом, металл реагирует с хлором, образуя хлорид металла, а водород выделяется наиболее активным металлом.
3. Металлический блеск: Многие металлы имеют характерный металлический блеск, который может измениться после взаимодействия с хлороводородом. При реакции с хлороводородом, металл может образовывать хлорид, который обладает другими оптическими свойствами, например, может быть белым или даже безцветным.
4. Реакция с газами: Хлороводород может реагировать не только с металлами, но и с некоторыми газами. Например, с хлором, бромом или йодом. В таких реакциях образуются соответствующие галогениды водорода (хлорид водорода, бромид водорода, йодид водорода).
5. Реакция с неметаллами: Хлороводород также может реагировать с некоторыми неметаллами, например, серой или фосфором. В результате образуются соответствующие кислоты – сероводород и фосфорная кислота.
Факторы, влияющие на реакцию HCl с металлами

Взаимодействие металлов с соляной кислотой (HCl) является одной из наиболее распространенных реакций в химии. Однако, ускорение или замедление данной реакции может зависеть от нескольких факторов.
Реактивность металла: Скорость реакции HCl с металлами зависит от их реактивности. Чем выше реактивность металла, тем быстрее протекает реакция. Например, алюминий и цинк очень реактивные металлы и реагируют с HCl мгновенно, образуя пузырьки водорода и соли металла. В то же время, медь и серебро являются менее реактивными и реагируют с HCl гораздо медленнее.
Концентрация соляной кислоты: Концентрация HCl влияет на скорость реакции с металлами. Чем выше концентрация кислоты, тем быстрее протекает реакция. Это связано с тем, что более концентрированная кислота обеспечивает большую количество ионов H+, которые участвуют в реакции с металлом.
Поверхностная область металла: Реакция HCl с металлами может протекать быстрее, если поверхность металла увеличивается. Например, если металл находится в порошкообразной форме, реакция может быть более интенсивной, поскольку большая поверхность металла обеспечивает большую активность для взаимодействия с HCl.
Температура: Высокая температура может значительно ускорить реакцию HCl с металлами. Повышение температуры может увеличить кинетическую энергию молекул, что способствует возникновению более частых и успешных столкновений между металлом и кислотой.
Последовательность реактивности металлов: В реакции HCl с смесью металлов, более реактивные металлы могут сначала реагировать, а менее реактивные - позже. Например, при добавлении различных металлических клиньев в HCl, алюминий реагирует первым, а затем цинк и медь.
Форма металла: Форма и состояние металла также могут влиять на скорость реакции с HCl. Например, если металл находится в виде проволоки или куска, то реакция может протекать медленнее, поскольку только поверхностные слои металла обеспечивают активность для взаимодействия с кислотой.
Выводы: Взаимодействие HCl с металлами зависит от ряда факторов, включая реактивность металла, концентрацию кислоты, поверхностную область металла, температуру, последовательность реакции металлов и форму металла. Учет этих факторов позволяет контролировать скорость и эффективность реакции HCl с металлами в различных условиях.
Практическое применение реакции HCl с металлами

Реакция HCl с металлами находит широкое применение в различных отраслях промышленности и научных исследованиях. Прежде всего, эта реакция используется для получения хлоридов металлов, которые являются важными химическими веществами и используются в различных производственных процессах. Хлориды металлов широко применяются в производстве металлургических материалов, лаков, красок, пластмасс, водопроводных труб и других изделий.
Кроме того, реакция HCl с металлами используется в аналитической химии для определения присутствия и концентрации различных металлов в образцах. Эта реакция позволяет провести качественный и количественный анализ металлических проб, что является важным для определения и контроля состава различных материалов и соединений.
Также, реакция HCl с металлами применяется в процессе очистки и нейтрализации различных отходов и сточных вод, содержащих металлы. С помощью данной реакции можно удалить из отходов тяжёлые металлы, такие как свинец, медь, ртуть и др., снизив тем самым их токсичность и вредность для окружающей среды.
В лаборатории реакция HCl с металлами применяется для получения газовых продуктов. Например, при реакции HCl с цинком выделяется водород, который широко используется в химической промышленности и других отраслях экономики. Получение водорода является важным шагом во многих процессах синтеза и производства различных химических соединений и веществ.
Таким образом, реакция HCl с металлами имеет значительное практическое применение в различных сферах деятельности, начиная от производства химических веществ до анализа материалов и очистки сточных вод. Эта реакция является важным инструментом для получения нужных продуктов и определения состава различных образцов и материалов.
Вопрос-ответ

Каким образом происходит взаимодействие HCl с металлами?
Взаимодействие HCl с металлами происходит путем образования солей металлов и выделения водорода.
Какие реакции могут происходить между HCl и металлами?
С реакцией HCl с металлами могут происходить такие реакции, как образование солей металлов и выделение водорода.
Какие свойства проявляет HCl при взаимодействии с металлами?
HCl обладает свойством образования солей металлов и выделения водорода при взаимодействии с металлами.
Как можно описать реакцию HCl с металлами?
Реакция HCl с металлами можно описать как процесс образования солей металлов и выделения водорода.
Что происходит при взаимодействии HCl с металлами?
При взаимодействии HCl с металлами происходит образование солей металлов и выделение водорода.