Алюминий, химический элемент с атомным номером 13, известен своей способностью образовывать оксидные пленки на своей поверхности при взаимодействии с кислородом. Эта реакция является одной из основных химических реакций алюминия и обеспечивает ему защиту от дальнейшей коррозии.
Реакция алюминия с кислородом происходит путем окисления металла до формирования оксида алюминия (Al2O3). В результате этой реакции молекулы кислорода (O2) проникают в структуру алюминия и вступают в химическую связь с его атомами. Образование оксида алюминия происходит на поверхности металла и возникает прочная защитная пленка, способная предотвращать дальнейшую коррозию и разрушение алюминиевой структуры.
Оксид алюминия является диэлектриком и обладает высокой прочностью, что обуславливает его широкое применение в различных отраслях промышленности, включая производство электроники, керамики, стекла и многое другое. Пленка оксида алюминия также обладает хорошей адгезией к алюминиевой поверхности, что делает ее стабильной и устойчивой к механическим воздействиям.
Таким образом, реакция алюминия с кислородом и образование оксида металла играют важную роль в обеспечении защиты алюминиевых конструкций от коррозии и повреждений. Это позволяет использовать алюминий в различных сферах, где требуются металлические материалы с высокой стойкостью к воздействию окружающей среды.
Реакция алюминия с кислородом

Алюминий - это легкий металл, который обладает высокой реакционной способностью, включая способность образовывать соединения с кислородом. Когда алюминий вступает в контакт с кислородом, происходит химическая реакция, в результате которой образуется оксид алюминия.
Реакция алюминия с кислородом можно описать следующим образом:
- Алюминий (Al) + Кислород (O2) → Оксид алюминия (Al2O3)
Реакция происходит с выделением большого количества энергии в виде тепла и света. Кроме того, она протекает очень быстро и возможна только при наличии кислорода. Поверхностный слой алюминия при реакции с кислородом покрывается оксидной пленкой, которая предотвращает дальнейшее окисление металла.
Оксид алюминия обладает высокой термической и химической стабильностью, что делает его полезным материалом в различных областях. Например, оксид алюминия используется в производстве абразивов, керамики, стекла и алюминиевых сплавов. Кроме того, он используется в качестве катализатора при различных химических реакциях.
В заключение, реакция алюминия с кислородом является важным химическим процессом, который приводит к образованию оксида алюминия. Эта реакция имеет большое значение в промышленности и науке, и находит применение во многих сферах человеческой деятельности.
Взаимодействие алюминия и кислорода
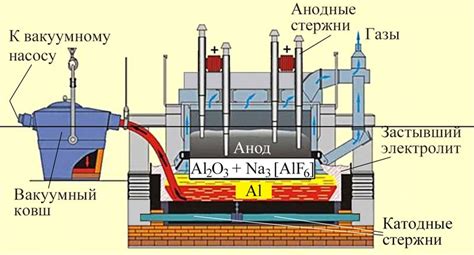
Алюминий является одним из самых распространенных химических элементов на Земле. Он особенно активно взаимодействует с кислородом, что приводит к образованию оксида алюминия (Al2O3). Это взаимодействие происходит в том числе и на поверхности алюминия при воздействии кислородного воздуха.
При контакте алюминия с кислородом происходит окисление металла, образуя пленку оксида на его поверхности. Такая пленка обладает высокой степенью стойкости и предотвращает дальнейшее окисление алюминия.
Защитная пленка оксида алюминия имеет значительную толщину и обладает хорошей адгезией к поверхности металла. Благодаря этому, алюминий обладает стойкостью к различным атмосферным условиям и не подвержен коррозии в сравнении с другими металлами.
Оксид алюминия обнаруживает высокую степень твердости, а также высокую точку плавления и пониженную проводимость электричества. Эти свойства делают его полезным материалом в производстве различных изделий и конструкций.
Оксид алюминия - продукт реакции
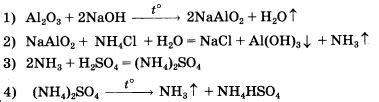
Оксид алюминия, также известный как криолит, является важным продуктом реакции между алюминием и кислородом. Эта реакция происходит при достаточно высоких температурах и обеспечивает алюминию защитный слой оксида.
Оксид алюминия представляет собой белый, химически инертный порошок, с хорошей термической и электрической проводимостью. Этот оксид обладает высокой теплоизоляцией и имеет широкий спектр применения в промышленности.
Оксид алюминия играет важную роль в процессе производства алюминия. Он формирует защитную пленку на поверхности металла, которая предотвращает дальнейшую реакцию с кислородом воздуха. Благодаря этому оксиду алюминий обладает высокой устойчивостью к коррозии и придаёт металлу прочность и долговечность.
Кроме того, оксид алюминия находит широкое применение в промышленности, включая производство керамики, стекла, абразивных материалов и электролитических конденсаторов. Этот материал также применяется в медицине в качестве компонента стоматологических материалов и протезов.
Следовательно, оксид алюминия является важным продуктом реакции между алюминием и кислородом. Этот химически стабильный и полезный продукт используется в различных отраслях промышленности и играет важную роль в производстве алюминия.
Описание свойств оксида металла
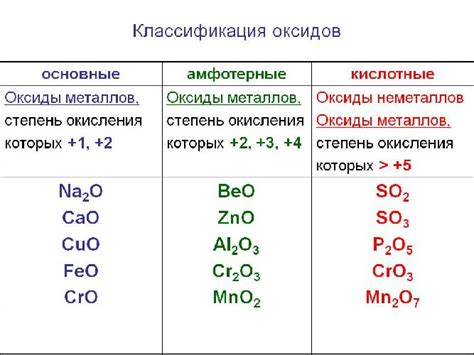
Оксид металла представляет собой химическое соединение, образующееся в результате реакции металла с кислородом. Это типичное явление, которое наблюдается при воздействии атмосферного кислорода на поверхность металла.
Оксиды металлов обладают рядом характерных свойств:
- Твердость и кристаллическая структура: оксиды металлов часто образуют кристаллические соединения с определенной распределенной симметрией. Это свойство определяет их твердость и структуру.
- Проводимость электричества: многие оксиды металлов обладают проводящими свойствами, что делает их полезными для применения в электротехнике и электронике.
- Теплопроводность: некоторые оксиды металлов хорошо проводят тепло, что делает их востребованными в промышленности, где требуется материал с высокой теплопроводностью.
- Химическая реактивность: оксиды металлов могут быть реактивными и обладать способностью взаимодействовать с другими веществами, что может привести к образованию новых соединений и изменению свойств оксида.
В зависимости от комбинации элементов, оксиды металлов могут иметь различные цвета и физические свойства. Например, оксид алюминия, известный также как корунд, может быть прозрачным и иметь высокую прочность, что делает его одним из самых важных материалов в индустрии.
Применение оксида алюминия
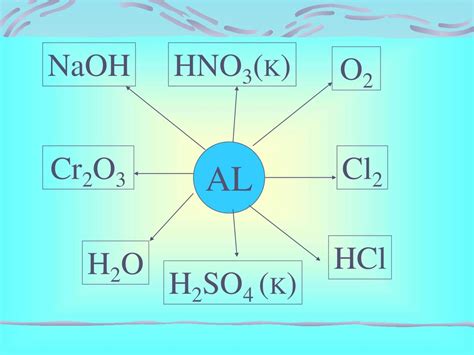
Оксид алюминия, также известный как алумина или алюминиевая керамика, имеет широкий диапазон применений в различных областях.
В силу своих физических и химических свойств, оксид алюминия широко используется в производстве огнеупорных материалов. Он обладает высокой стойкостью к высоким температурам и способностью сохранять свою прочность и форму при экстремальных условиях.
Кроме того, оксид алюминия имеет хорошие диэлектрические свойства, что делает его идеальным материалом для изготовления изоляторов и наполнителей для электронных устройств. Он обладает высокой стойкостью к перегрузкам, устойчив к электромагнитным полям и не проводит электричество.
Оксид алюминия также используется в промышленности в качестве абразивного материала. Он является основным компонентом шлифующих и полировальных средств, таких как шлифовальные круги, ленты и порошки. Благодаря своей твердости и износостойкости, оксид алюминия способен эффективно шлифовать различные поверхности и удалить старые покрытия или загрязнения.
Более того, оксид алюминия широко используется в производстве керамических изделий. Он обладает отличными теплоизолирующими свойствами, что делает его прекрасным материалом для изготовления керамической посуды, кафельной плитки и других керамических изделий. Кроме того, оксид алюминия может быть дополнительно модифицирован для получения различных цветов и текстур, что позволяет создавать разнообразные дизайны и украшения.
В целом, оксид алюминия является важным и многообластным материалом, который находит широкое применение в различных отраслях промышленности, начиная от строительства и электроники, и заканчивая производством керамики и абразивных материалов.
Вопрос-ответ

Что происходит при реакции алюминия с кислородом?
При реакции алюминия с кислородом образуется оксид металла - алюминиевый оксид Al2O3.
Какие условия необходимо создать для проведения реакции алюминия с кислородом?
Для проведения реакции алюминия с кислородом необходимо обеспечить наличие кислорода, температуру выше точки плавления алюминия (660°C) и желательно использовать порошкообразную форму алюминия для увеличения скорости реакции.
Какова химическая формула алюминиевого оксида, образующегося при реакции?
Химическая формула алюминиевого оксида - Al2O3. В молекуле алюминиевого оксида два атома алюминия соединяются с тремя атомами кислорода.
