Валентность металлов может быть одним из важных параметров для их химических свойств. Для металлов, таких как калий (K) и барий (Ba), валентность можно определить через соединения, которые они образуют с гидроксидами.
Гидроксид калия (KOH) образуется путем реакции металла калия с водой. Это бесцветное вещество, обладающее щелочными свойствами. В спецификации формулы KOH, в исправленой формуле KL1(H2L2)3, основание (KL1) увязывается с тремя кислородными атомами (H2L2). То есть валентность калия равна 1.
Барий гидроксид (BaOH2) образуется, когда металл бария реагирует с водой. Это белое вещество, также обладает щелочными свойствами. В формуле BaOH2, основание (Ba) увязывается с двумя кислородными атомами (OH2). То есть валентность бария равна 2.
Валентность металлов KOH и BaOH определяется через соединения, которые они образуют с гидроксидами. Для калия (K) валентность равна 1, так как в формуле KOH имеется одно основание, связывающееся с тремя кислородными атомами. Для бария (Ba) валентность равна 2, так как в формуле BaOH2 имеется одно основание, связывающееся с двумя кислородными атомами.
Валентность металлов KOH, BaOH

Металлы - это элементы химического периодического стола, которые обладают свойствами металлического гланка и хорошей тепло- и электропроводностью. В химических реакциях металлы могут образовывать различные соединения, в том числе и с щелочами, такими как гидроксиды.
Гидроксиды - это неорганические соединения, в состав которых входит группа OH-, называемая гидроксильной группой. Одним из примеров гидроксидов является гидроксид калия (KOH) и гидроксид бария (BaOH).
Валентность металлов в гидроксидах определяется по следующим правилам:
- Валентность калия (K) в гидроксиде калия (KOH) равна 1.
- Валентность бария (Ba) в гидроксиде бария (BaOH) также равна 2.
Это обусловлено тем, что калий находится в первой группе периодической системы, у которой валентность равна номеру группы (группа 1 - валентность 1), а барий находится во второй группе, у которой валентность равна номеру группы (группа 2 - валентность 2).
Зная валентность металлов KOH и BaOH, мы можем определить стехиометрическую формулу гидроксида и соотношение между металлом и гидроксильной группой. Например, в гидроксиде калия один атом калия соединяется с одной гидроксильной группой, а в гидроксиде бария один атом бария соединяется с двумя гидроксильными группами.
Понятие валентности металлов
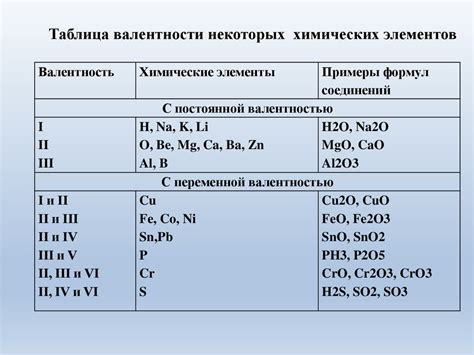
Валентность металлов – это количество электронов, которые металл способен отдать или принять при взаимодействии с другими элементами. Она определяется расположением элемента в периодической системе химических элементов и позволяет определить химические свойства металла.
Валентность металлов может быть как постоянной, так и переменной. Постоянная валентность означает, что металл всегда отдает или принимает одно и то же количество электронов при вступлении в химическую реакцию, например, Na (натрий) всегда имеет валентность +1. Переменная валентность означает, что металл может изменять количество отдаваемых или принимаемых электронов, например, железо (Fe) имеет валентность +2 и +3.
Определение валентности металлов позволяет предсказывать тип химической связи и химические соединения, которые металл может образовать. Например, металл с валентностью +2 будет формировать ионы с двумя положительными зарядами, а металл с валентностью +3 будет формировать ионы с тремя положительными зарядами.
Конкретные значения валентности металлов могут быть представлены в виде таблицы, где перечислены элементы и их валентность. Например:
| Металл | Валентность |
|---|---|
| Натрий (Na) | +1 |
| Железо (Fe) | +2, +3 |
| Калий (K) | +1 |
Зная валентность металлов, ученые и химики могут предсказать реакции, образование соединений и свойства веществ, что является важным в химической науке и промышленности.
Валентность металла КОН

Валентность металла KOH определяется его способностью образовывать соединения с отрицательно заряженными ионами гидроксида (OH-). В случае металла Калия (K) в соединении KOH валентность металла составляет +1, что означает, что он может потерять один электрон и образовать положительно заряженный ион K+. Таким образом, валентность металла КОН равна +1.
Калий является щелочным металлом и образует стабильные соединения с гидроксидом (OH-) при диссоциации молекулы KOH. Металл Калий обладает одним внешним электроном в своей валентной оболочке, который он может потерять, образуя положительно заряженный ион. Таким образом, валентность металла KOH равна +1.
В соединениях с металлом Калия обычно встречается одно- валентное окисление металла KOH, что объясняется его способностью образовывать одно молекулярное соединение при диссоциации гидроксида KOH.
Таким образом, валентность металла КОН составляет +1 и определяется его способностью образовывать положительно заряженные ионы Калия (K+).
Влияние валентности металла КОН на его химические свойства
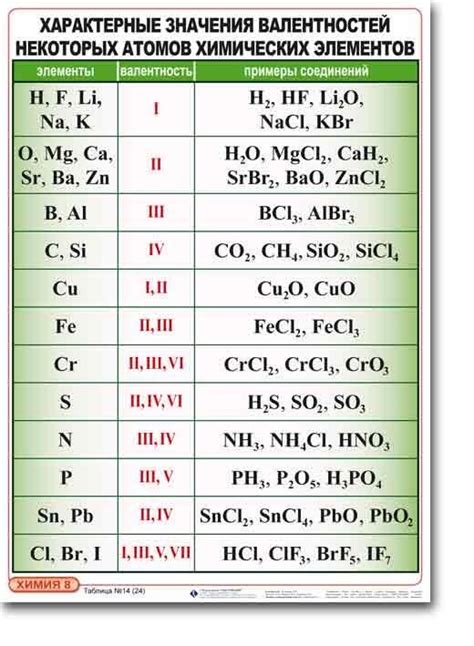
Валентность металла KOH оказывает значительное влияние на его химические свойства. KOH является ионным соединением, где катионом выступает металл, а анионом - гидроксид. Валентность металла определяет количество электронов, которые он способен отдавать или принимать в процессе химических реакций.
Высокая валентность металла KOH может сказаться на его реакционной способности. Например, если валентность металла равна 2, то он может образовывать соединения с двумя атомами гидроксида. Это отражается на его растворимости в воде, а также на химических свойствах его соединений.
Металл KOH с низкой валентностью может образовывать соединения с одним атомом гидроксида. Такие соединения обычно обладают другими химическими свойствами, чем соединения с металлом KOH с более высокой валентностью.
Важно отметить, что валентность металла KOH может быть изменена в различных условиях эксперимента, что также может повлиять на его химические свойства. Например, при изменении pH среды или введении дополнительных веществ.
Таким образом, валентность металла KOH является важным параметром, определяющим его химические свойства и реакционную способность. Это позволяет использовать металл KOH в различных областях, таких как производство щелочных растворов, промышленность и медицина.
Валентность металла BaOH
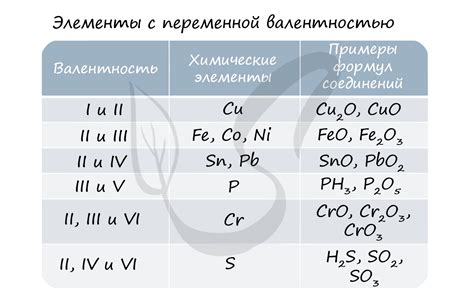
Барий является алкалиноземельным металлом, который имеет валентность +2. Это означает, что он может образовывать соединения, в которых он передает два электрона другим элементам или группам элементов.
Когда барий реагирует с гидроксидом калия (KOH), он передает два электрона калию, образуя соединение BaOH. В этом соединении барий находится в окислительном состоянии +2, а калий - в окислительном состоянии -1. Таким образом, барий имеет валентность +2 в соединении BaOH.
Однако барий также может образовывать соединения с другими элементами, в которых его валентность может быть и +1. Например, с атомами хлора барий образует соединение BaCl, в котором барий имеет валентность +1.
Валентность металла BaOH зависит от соединяющегося с ним элемента или группы элементов и может быть разной. Варианты валентности - +1 и +2 - определяются его электронной конфигурацией и способностью передавать электроны другим элементам.
Различия валентности металлов KOH и BaOH

Металлы KOH и BaOH обладают различной валентностью, что влияет на их физические и химические свойства. Рассмотрим основные отличия между ними.
1. Калий и барий. KOH содержит калий (K), а BaOH - барий (Ba). Калий и барий принадлежат к разным группам в периодической системе элементов и имеют разные химические свойства.
2. Окислители и основания. KOH является сильным основанием, а BaOH - сильным окислителем. Это связано с разной валентностью металлов. Калий (K) в KOH имеет валентность +1, а барий (Ba) в BaOH - +2.
3. Реакции окисления и восстановления. Из-за различной валентности металлов, KOH и BaOH обладают разной способностью окислять и восстанавливаться. KOH может вступать в реакции окисления, тогда как BaOH обычно проявляет свои свойства как окислитель.
4. Растворимость в воде. KOH лучше растворяется в воде за счет наличия катиона K+ с меньшим зарядом. Бах легче образует осадок, так как барий (Ba2+) имеет больший заряд, который притягивает большее количество отрицательно заряженных ионов из раствора.
5. Использование в промышленности. Из-за разных свойств и валентности металлов, KOH и BaOH находят применение в разных областях промышленности. KOH используется в производстве мыла, как щелочное основание в химической промышленности и в процессе электролиза. BaOH применяется для получения барий-сульфата, добавки в стекло и керамику, а также в производстве электронных устройств и аккумуляторов.
Вопрос-ответ

Какова валентность металла в соединении KOH?
В соединении KOH валентность калия (K) равна 1+, а валентность гидроксильной группы (OH) равна 1-. Поэтому общая валентность KOH составляет 1+ - 1- = 0.
Какова валентность металла в соединении BaOH?
В соединении BaOH валентность бария (Ba) равна 2+, а валентность гидроксильной группы (OH) равна 1-. Поэтому общая валентность BaOH составляет 2+ - 1- = 1+.
Почему валентность металла в KOH равна 1+?
Валентность металла в соединении KOH определяется его электрохимическим потенциалом, а именно потерей одного электрона. Калий имеет один электрон на внешнем энергетическом уровне, поэтому он готов отдать его, чтобы достичь стабильной восьмеричной валентной оболочки. В результате калий становится одновалентным с положительным зарядом 1+.
Какая роль гидроксильной группы (OH) в определении валентности металла?
Гидроксильная группа (OH) в определении валентности металла играет роль отрицательного иона с валентностью 1-. При соединении гидроксильной группы с металлом, его валентность определяется по принципу сохранения заряда: валентность металла будет равна противоположной по знаку валентности гидроксильной группы.
Как определить общую валентность соединения BaOH?
Общая валентность соединения BaOH определяется путем сложения валентности металла (бария) и валентности гидроксильной группы (OH). В данном случае валентность бария равна 2+, а валентность гидроксильной группы равна 1-. Поэтому общая валентность BaOH составляет 2+ - 1- = 1+.
