Серная кислота является одним из наиболее распространенных и важных химических веществ. Сочетание серной кислоты с металлами порождает реакции, которые отличаются своими особенностями и имеют различные применения.
Взаимодействие металлов с серной кислотой основывается на образовании реакционного продукта - солей серной кислоты. При этом, характер взаимодействия зависит от активности металла и его электрохимического потенциала.
Сильные электронно-акцепторные свойства серной кислоты позволяют ей разрушать окислительную плёнку, которая обычно образуется на поверхности металла. Это позволяет серной кислоте реагировать с различными металлами и даже продолжать реакцию с образованием газа в виде водорода. Взаимодействие металлов с серной кислотой может использоваться в различных процессах, например, в осаждении металлов, очистке поверхностей от окислительных слоев и т.д.
Устойчивость металлов к серной кислоте

Устойчивость металлов к серной кислоте является важным аспектом взаимодействия этих материалов. Известно, что некоторые металлы проявляют сильную реакцию на воздействие серной кислоты, в то время как другие обладают высокой устойчивостью к ней.
Одним из металлов с низкой устойчивостью к серной кислоте является железо. При взаимодействии с серной кислотой на поверхности железа образуется слой серы и обнажается металлическая поверхность. Этот процесс называется коррозией. Чтобы предотвратить коррозию железа в серной кислоте, возможно использование защитных покрытий или специальных легированных сталей, обладающих повышенной устойчивостью.
С другой стороны, алюминий является металлом с высокой устойчивостью к серной кислоте. Это связано с тем, что на поверхности алюминия образуется пленка оксида, которая действует как защитный барьер и предотвращает дальнейшую реакцию металла с кислотой. Эта пленка защищает алюминий от коррозии и обеспечивает его долговечность при взаимодействии с серной кислотой.
Кроме железа и алюминия, есть и другие металлы, которые проявляют различную степень устойчивости к серной кислоте. Например, медь обладает высокой устойчивостью к серной кислоте, благодаря образованию защитного слоя оксида на ее поверхности. Однако, некоторые металлы, такие как цинк и свинец, реагируют с серной кислотой с образованием солей и высвобождением газа.
Устойчивость металлов к серной кислоте является важным параметром при выборе материала для технических и промышленных целей. Правильный выбор металла позволяет обеспечить долговечность и надежность конструкций при взаимодействии с серной кислотой, а также избежать возможных аварийных ситуаций.
Влияние структуры металла

Структура металла имеет существенное влияние на его взаимодействие с серной кислотой. Основным фактором, определяющим реакционную способность металлов, является их кристаллическая решетка.
При взаимодействии с серной кислотой, металлы могут образовывать сульфаты с различной степенью растворимости. Это обусловлено не только химическими свойствами металла, но также его кристаллической структурой. Например, в случае чистого железа, его решетка обладает высокой плотностью упаковки атомов, что делает его более устойчивым к разрушению в кислой среде.
Помимо кристаллической структуры, влияние на взаимодействие с серной кислотой также оказывает примесные элементы в металле. Например, в случае стали, содержащей хром, происходит образование защитной пассивной пленки на поверхности металла, которая предотвращает его дальнейшее разрушение под влиянием кислоты.
Таким образом, структура металла играет важную роль в его взаимодействии с серной кислотой. Понимание этих особенностей позволяет эффективно использовать металлы в различных промышленных процессах, таких как производство удобрений, нефтепереработка и другие.
Электрическая потенциал металла
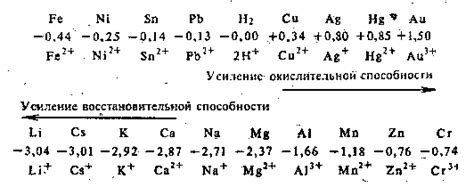
Электрический потенциал металла - это величина, которая характеризует способность металла удерживать или отдавать электроны. Она является мерой энергии, необходимой для перемещения единичного положительного заряда от бесконечности до поверхности металла.
Каждый металл обладает своим уникальным электрическим потенциалом, который определяется его химическими свойствами и структурой кристаллической решетки. Величина электрического потенциала может быть положительной или отрицательной и измеряется в вольтах.
Электрический потенциал металла является важным параметром при взаимодействии металла с серной кислотой. При контакте металла со средой, в данном случае серной кислотой, происходит трансфер электронов между металлом и реагентами. Электрический потенциал металла определяет направление этого трансфера, влияя на протекание реакции.
Зная электрический потенциал металла, можно определить его реакционную активность и способность вступать в химические реакции. Это позволяет использовать металлы с различными электрическими потенциалами для конкретных целей, например, в процессе электролиза, гальванических элементах или при создании различных электрохимических устройств.
Концентрация серной кислоты

Концентрация серной кислоты - это важный параметр, определяющий химические свойства и взаимодействие данного вещества с другими веществами. Концентрация характеризует количество серной кислоты, содержащейся в единице объема или массы раствора.
Обычно концентрацию серной кислоты выражают в процентах, молях или граммах на литр раствора. Выбор определенной концентрации зависит от требуемых условий реакции, желаемой селективности и эффективности процесса.
Высокая концентрация серной кислоты обеспечивает быстрое и интенсивное взаимодействие с металлами. Она может использоваться для аналитических, синтетических и технологических целей, например, при выделении металлов из руды или в процессе обработки материалов на промышленных предприятиях.
Низкая концентрация серной кислоты может применяться в более мягких условиях, например, для удаления ржавчины с поверхности металла или очистки деталей. В таком случае, процесс реакции может занимать больше времени, но он будет менее агрессивным по отношению к самих металлов.
При выборе концентрации серной кислоты необходимо учитывать характеристики металла, его чувствительность к окислению и другим химическим реакциям. Важно также учитывать безопасность работы с серной кислотой и соблюдать соответствующие меры предосторожности.
Температура взаимодействия

Взаимодействие металлов с серной кислотой происходит при повышенных температурах. Точная температура зависит от типа металла и его химических свойств.
Например, низкотемпературное взаимодействие меди с серной кислотой начинается при температуре от 50 градусов Цельсия. При этой температуре серная кислота активно взаимодействует с поверхностью меди, образуя соединения меди(II) с серной кислотой, такие как медный сульфат (CuSO4).
Взаимодействие железа и серной кислоты начинается при более высоких температурах - от 200 градусов Цельсия. При этой температуре серная кислота окисляет железо, превращая его в желез(III) сульфат (Fe2(SO4)3). Также возможно образование сернистого аниона (SO3)2- и серного аниона (SO4)2-.
Взаимодействие алюминия с серной кислотой происходит при еще более высоких температурах - около 600 градусов Цельсия. При этой температуре серная кислота окисляет алюминий, превращая его в алюминий(III) сульфат (Al2(SO4)3). Отметим, что алюминий обладает повышенной устойчивостью к окислительным воздействиям и серной кислоте.
Процессы при взаимодействии металлов и серной кислоты
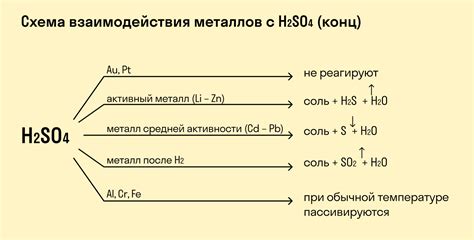
Химическое взаимодействие металлов и серной кислоты является одним из важных процессов в химии. При контакте металла с серной кислотой происходит реакция, в ходе которой образуются новые вещества и выделяется водород.
Большинство металлов реагируют с серной кислотой, но скорость реакции и степень ее полноты зависят от свойств металла и концентрации серной кислоты. Некоторые металлы, такие как железо и цинк, реагируют с серной кислотой достаточно активно, образуя соли соответствующих металлов и выделяя большое количество водорода.
Реакция металлов с серной кислотой включает несколько этапов. Сначала металл активно взаимодействует с серной кислотой, образуя сульфат металла и выделяя водород. Далее происходит дальнейшее окисление металла с образованием оксидов металла, которые растворяются в серной кислоте, образуя соли.
Процесс взаимодействия металлов и серной кислоты имеет широкое применение в промышленности и лабораторных условиях. Например, такая реакция используется для очистки поверхности металлических изделий от загрязнений и ржавчины. Металлы также могут быть использованы в качестве катализаторов при реакциях, в которых основным веществом является серная кислота.
Образование сульфатов
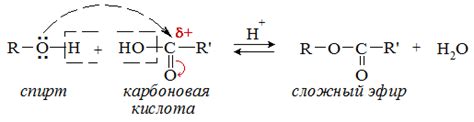
Взаимодействие металлов с серной кислотой приводит к образованию сульфатов. Сульфаты – это соли серной кислоты, состоящие из иона серы со степенью окисления +6 и металлического катиона.
Образование сульфатов характеризуется следующими особенностями:
- Реакция металла с серной кислотой происходит с образованием газа сероводорода (H2S) и соответствующего сульфата.
- Скорость реакций между металлом и серной кислотой зависит от их химической активности.
- Образование сульфата металла сопровождается изменением окраски раствора – он приобретает цвет, свойственный иону металла.
- Некоторые металлы способны образовывать двухвалентные сульфаты, в которых ион металла имеет степень окисления +2.
Формирование сульфатов имеет широкое применение в различных отраслях промышленности:
- Производство удобрений: сульфаты аммония, магния, калия и других металлов используются в качестве удобрений для повышения плодородия почвы.
- Гальванические процессы: сульфаты металлов, такие как медь, цинк и никель, применяются в электротехнике и электрохимии для создания покрытий и гальванической обработки поверхностей.
- Производство красителей: некоторые сульфаты металлов служат сырьем для получения пигментов и красителей для различных отраслей промышленности, включая текстильное и пищевое производство.
Выделение газов

Взаимодействие металлов с серной кислотой часто сопровождается выделением газов. Одним из наиболее распространенных газов при данной реакции является водород. Многие металлы, такие как цинк, железо, медь, алюминий, магний и другие, способны образовывать гидроксиды и сульфаты, освобождая при этом водород. Это происходит из-за реакции металла с серной кислотой, в результате которой образуется сульфат металла и вода.
Также при взаимодействии некоторых металлов с серной кислотой может выделяться диоксид серы. Например, при реакции железа с концентрированной серной кислотой образуется сульфат железа(II) и выделяется диоксид серы. Диоксид серы представляет собой газ со специфическим запахом, который обладает окислительными свойствами и может быть использован в различных химических процессах.
Выделение газов при взаимодействии металлов с серной кислотой имеет практическое применение. Например, выделение водорода может использоваться в процессе производства водородных топливных элементов. Диоксид серы, в свою очередь, может быть использован в синтезе серных кислот и других химических соединений.
Ионные реакции

Ионные реакции – это химические реакции, в которых происходит образование или разрушение ионов. Взаимодействие металлов с серной кислотой является примером ионных реакций.
При взаимодействии металлов с серной кислотой происходит образование солей и выделение водорода. Металл реагирует с кислотой, отдавая свои электроны, которые образуют ионы металла. Водород и ионы из кислоты образуют молекулы воды.
Эти ионные реакции имеют несколько особенностей. Во-первых, реакция происходит только тогда, когда металл активнее водорода. Например, железо или цинк реагируют с серной кислотой, а медь или серебро - нет. Во-вторых, скорость реакции зависит от концентрации кислоты и поверхности металла. Чем выше концентрация кислоты и чем больше площадь поверхности металла, тем быстрее протекает реакция.
Ионные реакции металлов с серной кислотой имеют широкое применение. Одним из важных применений является получение водорода. Водород используется в различных отраслях промышленности, в том числе в производстве аммиака, синтезе полимеров и производстве взрывчатых веществ. Кроме того, соли, образующиеся в результате реакции, также имеют практическое применение, например, серная кислота используется в производстве удобрений и в химической промышленности.
Применение взаимодействия металлов с серной кислотой
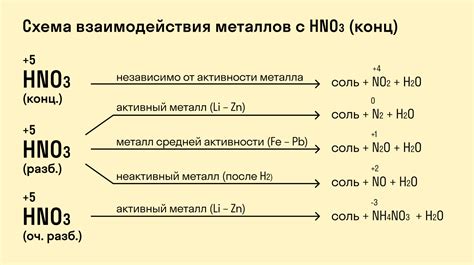
Металлы являются одной из основных групп химических элементов и находят широкое применение в различных отраслях промышленности. Один из способов взаимодействия металлов с химическими веществами - это реакция с серной кислотой. Серная кислота (H2SO4) является одной из наиболее распространенных кислот и используется в множестве процессов.
Применение взаимодействия металлов с серной кислотой обусловлено несколькими факторами. Во-первых, такое взаимодействие позволяет получать соединения металлов, которые имеют различные применения. Например, реакция алюминия с серной кислотой приводит к образованию алюминия сульфата, который используется в качестве сырья для производства алюминия и его соединений.
Во-вторых, взаимодействие металлов с серной кислотой может использоваться для очистки металлических поверхностей от оксидов и других загрязнений. Серная кислота обладает хорошей растворимостью, что позволяет эффективно удалять нежелательные отложения с поверхности металла. Например, реакция железа с серной кислотой позволяет удалить оксиды железа, придавая поверхности металла металлический блеск.
В-третьих, взаимодействие металлов с серной кислотой может быть использовано в процессах синтеза и получения различных соединений. Например, реакция цинка с серной кислотой позволяет получить цинковый сульфат, который широко используется в гальваническом производстве и сельском хозяйстве в качестве удобрения.
Вопрос-ответ

Какие металлы реагируют с серной кислотой?
Серная кислота реагирует с многими металлами, такими как цинк, железо, алюминий, никель, свинец и др.
Что происходит при реакции металлов с серной кислотой?
При взаимодействии металлов с серной кислотой происходит образование солей серной кислоты и выделение водорода.
Какие особенности имеет взаимодействие алюминия с серной кислотой?
Взаимодействие алюминия с серной кислотой происходит с образованием соли серной кислоты и выделением сернокислого газа, который образует характерный запах.
В каких областях применяется реакция металлов с серной кислотой?
Реакция металлов с серной кислотой применяется в химическом производстве для получения солей серной кислоты, а также для производства водорода и очистки от него газов.
