Металлы – это особая группа химических элементов, характеризующаяся своими уникальными физическими и химическими свойствами. Один из важных аспектов реактивности металлов – их взаимодействие с кислотами. Кислоты, обладая выраженной кислотностью, способны вызвать химическую реакцию с металлами, в результате которой происходит образование солей и выделение водорода.
Наличие кислотности позволяет кислотам совершать протонный перенос с молекулы к молекуле, что и вызывает реакцию с металлами. При этом, реакция настолько сильна, что может привести к растворению металла, образуя его ионы в растворе.
Взаимодействие металлов с кислотами характеризуется различными степенями активности металлов и реакционной способностью кислот. Существует таблица взаимодействия металлов с кислотами, которая показывает, какой металл будет активнее взаимодействовать с конкретной кислотой. Эта таблица позволяет прогнозировать реакционную способность металлов и предсказывать, какая смесь металла и кислоты приведет к образованию солей, а какая – к выделению водорода.
Металлы и кислоты: важное взаимодействие
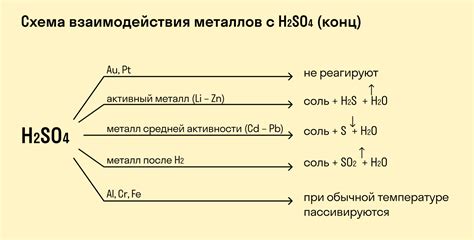
Металлы и кислоты взаимодействуют друг с другом, образуя соли и выделяя водород. Это является одним из основных процессов химических реакций. Взаимодействие металлов с кислотами основано на их активности, химических свойствах и электрохимическом потенциале.
Реакция металлов с кислотами происходит по следующей схеме: металл образует ион положительного заряда, который вытесняет водород из кислоты, образуя соль металла. При этом кислота теряет свои характерные кислотные свойства и становится солью.
Однако не все металлы реагируют с кислотами одинаково. Взаимодействие металлов и кислот зависит от их положения в электрохимическом ряде. Например, щелочные металлы, такие как натрий, калий и литий, очень активно взаимодействуют с кислотами и образуют соли. В то время как металлы серебро, золото, платина и другие инертные металлы не реагируют с большинством кислот.
Знание взаимодействия металлов с кислотами имеет большое значение в различных отраслях, включая металлургию, химию, фармацевтику и производство материалов. Кроме того, взаимодействие металлов с кислотами может использоваться для получения различных металлических солей, которые широко применяются в лабораториях и промышленности.
Реакция металлов с кислотами
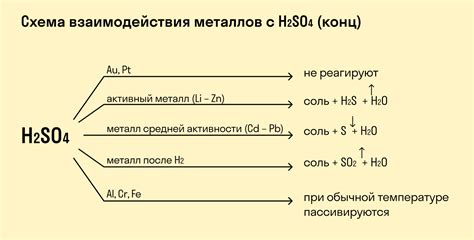
Металлы и кислоты могут взаимодействовать между собой, образуя различные химические реакции. При этом образуются соли и выделяется водород. Взаимодействие металлов и кислот может происходить только при наличии свободных отрицательных и положительных зарядов. Благодаря этому они образуют ионы, которые обеспечивают химическую реакцию.
Металлы реагируют с кислотами различным образом в зависимости от их активности. Для активных металлов, таких как натрий или калий, реакция происходит очень интенсивно, с выделением большого количества водорода. Это связано с тем, что активные металлы имеют большую способность отдавать электроны.
Менее активные металлы, такие как железо или цинк, реагируют с кислотами медленнее. Причина этого заключается в том, что они имеют меньшую способность отдавать электроны. Однако, они все равно могут образовывать ионы металла и соли, только реакция протекает медленнее и не так интенсивно.
Существуют также металлы, которые не реагируют с кислотами вообще. Примером может служить золото или платина. Это связано с их невысокой или отсутствующей активностью. Они не образуют ионов металла и солей в результате реакции с кислотами.
Взаимодействие металлов и кислот может иметь практическое применение. Например, реакция цинка с серной кислотой может использоваться для получения водорода. Кроме того, это явление важно для понимания причин коррозии металлов в присутствии кислот.
Кислоты и их химические свойства
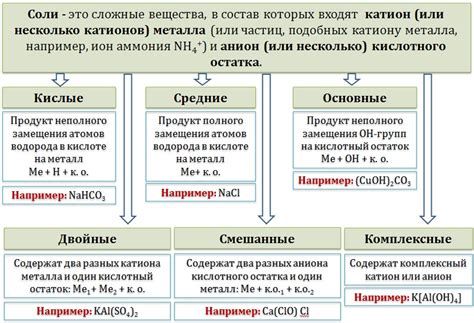
Кислоты – это химические соединения, обладающие кислотными свойствами, то есть способностью образовывать ион водорода (H+) в водном растворе. Кислоты могут быть органическими или неорганическими веществами.
Неорганические кислоты:
- Соляная кислота (HCl) – одна из самых распространенных неорганических кислот. Она является сильной кислотой и образует ионы H+ и Cl- в водном растворе. Соляная кислота реагирует с металлами, образуя соответствующие соли и выделяя водородный газ.
- Азотная кислота (HNO3) – это еще одна сильная неорганическая кислота, которая образует ионы H+ и NO3- в водном растворе. Азотная кислота используется в промышленности для производства удобрений и взрывчатых веществ.
- Фосфорная кислота (H3PO4) – это слабая кислота, которая образует три иона H+ и один ион PO4^3- в водном растворе. Фосфорная кислота используется в производстве удобрений, стекла и мыла.
Органические кислоты:
- Уксусная кислота (CH3COOH) – это слабая органическая кислота, которая образуется в результате брожения этилового спирта. Уксусная кислота используется в пищевой промышленности для консервирования и приготовления маринадов.
- Лимонная кислота (C6H8O7) – это слабая органическая кислота, которая является основным кислотным компонентом лимонного сока. Она широко используется в пищевой промышленности как консервант, а также в косметической и фармацевтической промышленности.
- Аминокислоты – это класс органических соединений, которые являются основными строительными блоками белков. Аминокислоты содержат карбоксильную группу (–COOH) и аминогруппу (–NH2), образуя двойственное кислотно-основное свойство.
Кислоты могут реагировать с металлами, основаниями и многими другими соединениями, проявляя свои химические свойства. Понимание этих свойств позволяет широко использовать кислоты в промышленности, научных исследованиях и повседневной жизни.
Таблица взаимодействий
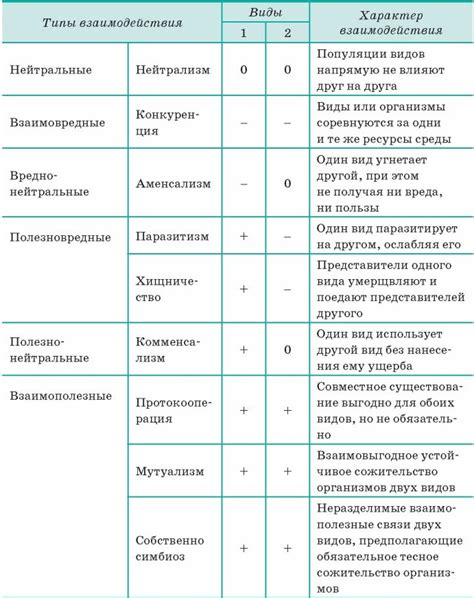
Металлы и кислоты являются важными и широко используемыми веществами в химии. Металлы могут реагировать с кислотами, образуя соли и выделяя водород. На основе этих реакций можно составить таблицу взаимодействий различных металлов с разными кислотами.
Таблица взаимодействий металлов с кислотами позволяет определить, какой металл будет реагировать с данной кислотой и образовывать соль и выделять водород. В таблице указываются названия металлов и кислот, а также происходящая реакция и образующиеся продукты.
Например, если взять металл алюминий (Al) и кислоту соляную (HCl), то произойдет реакция, при которой образуется соль алюминия (AlCl3) и выделяется водород (H2). Таким образом, можно сделать вывод, что алюминий реагирует с соляной кислотой.
Таблица взаимодействий металлов с кислотами помогает установить, какие комбинации металлов и кислот являются химически активными и могут производить реакции. Это имеет практическое значение при проведении экспериментов и в промышленности, где используются различные металлы и кислоты.
Металлы и их реакционная способность

Металлы - это элементы, которые обладают определенными характеристиками, такими как блеск, твердость и электропроводность. Взаимодействие металлов с другими веществами является важной химической реакцией, которая определяет их реакционную способность.
Металлы могут реагировать с различными веществами, включая кислоты. Реакция металлов с кислотами происходит с образованием соли и выделением водорода. Реакционная способность металлов может быть различной и зависит от их позиции в электрохимическом ряду.
Некоторые металлы, такие как литий, натрий и калий, обладают высокой реакционной способностью и могут реагировать с кислотами, даже с водой. Они активно выделяют водород и образуют соли. Другие металлы, такие как железо и цинк, реагируют с кислотами, но их реакционная способность не так высока.
Реакция металлов с кислотами может быть представлена в виде таблицы, в которой указаны металлы и их способность к реакции с различными кислотами. Зеленый цвет означает активное взаимодействие, красный - отсутствие реакции. Эта таблица может быть полезным инструментом для изучения реакционной способности металлов и предсказания характера их взаимодействия с кислотами.
| Металлы | Способность к реакции с кислотами |
|---|---|
| Литий | Активное взаимодействие |
| Натрий | Активное взаимодействие |
| Железо | Умеренное взаимодействие |
| Цинк | Умеренное взаимодействие |
| Серебро | Отсутствие реакции |
Изучение реакционной способности металлов и их взаимодействия с кислотами имеет большое значение для практики, так как позволяет предсказывать возможность реакции и разрабатывать новые материалы и технологии.
Практическое применение

Знание таблицы взаимодействий металлов с кислотами имеет практическое значение в различных областях науки и промышленности. В первую очередь, она широко используется в химической промышленности при производстве различных соединений на основе металлов. Зная, какой металл реагирует с определенной кислотой и в каких условиях, можно эффективно контролировать и оптимизировать процесс синтеза.
Кроме того, эта таблица находит применение в аналитической химии и исследовательских лабораториях. Например, при анализе состава металлических образцов необходимо знать, какие кислоты можно использовать для их растворения и извлечения нужных компонентов. Таблица позволяет выбрать подходящую кислоту, чтобы избежать нежелательных реакций или разрушения образца.
Также, знание взаимодействия металлов с кислотами важно для безопасной работы с химическими веществами. Работники, занимающиеся обработкой и хранением металлических материалов, должны быть осведомлены о возможных опасностях и правильных способах обращения с металлическими отходами. Таблица помогает оценить риск возникновения опасной реакции при хранении и транспортировке металлов.
В области образования таблица взаимодействий металлов с кислотами является важным учебным материалом. Студенты изучают эту таблицу, чтобы понять основные принципы реакций между металлами и кислотами, а также использовать полученные знания в лабораторной практике. Это позволяет им развить навыки экспериментальной работы и понимание основ химии.
Применение знаний о взаимодействии металлов и кислот

Знание отношений между металлами и кислотами имеет широкое применение в различных областях. Оно не только помогает понять химические процессы, но и находит своё применение в промышленности, медицине и экологии.
В промышленности знание этих взаимодействий позволяет производить различные процессы, такие как очистка металлов, получение солей или катализаторов. Также, оно является основой для разработки методов защиты металлических конструкций от коррозии.
В медицине эти знания часто используются при разработке лекарственных препаратов. Например, многие лекарства содержат металлы в своем составе, которые реагируют с кислотами в организме, образуя активные вещества.
В экологии знание взаимодействия металлов и кислот позволяет оценивать воздействие промышленных выбросов на окружающую среду. Например, зная, как металлы реагируют с кислотами, можно предсказать, какие ионы могут образовываться и как это может повлиять на состав воды и почвы.
Таким образом, знание о взаимодействии металлов и кислот имеет применение в различных областях, помогает понять химические процессы и находит применение в промышленности, медицине и экологии.
Важность и практическая значимость изучения реакции металлов с кислотами
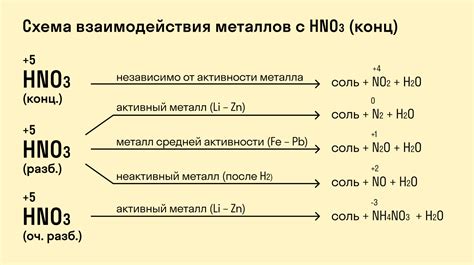
Изучение реакции металлов с кислотами имеет большую важность и практическую значимость в различных областях, таких как химическая промышленность, металлургия и экология.
В химической промышленности знание реакций металлов с кислотами позволяет определить возможности применения различных металлов в процессах синтеза и получения различных химических соединений. Например, знание реакции железа с соляной кислотой позволяет использовать его в производстве хлорида железа, который широко применяется в качестве коагулянта в водоподготовке и производстве бумаги.
В металлургии изучение реакций металлов с кислотами помогает определить стойкость и коррозионную устойчивость различных металлических материалов. На основе этих данных разрабатываются специальные защитные покрытия и легированные сплавы, которые могут быть использованы для создания более долговечных и надежных конструкций.
Изучение реакции металлов с кислотами имеет также важное значение для экологии. Оно позволяет оценить потенциальные риски различных металлических отходов, которые могут попадать в окружающую среду. Например, знание реакции меди с серной кислотой позволяет предсказать образование токсического вещества - сернистого газа. Эта информация может быть использована для разработки методов переработки и утилизации металлических отходов, снижения их влияния на окружающую среду и сохранения биоразнообразия.
Вопрос-ответ

Какие металлы могут реагировать с кислотами?
Многие металлы могут реагировать с кислотами. Некоторые из них включают в себя цинк, железо, медь, свинец и алюминий.
Что происходит, когда металл реагирует с кислотой?
При реакции металл с кислотой обычно происходит образование соли и выделение водорода. Например, когда цинк реагирует с соляной кислотой, образуется хлорид цинка и выделяется водородный газ.
Какие результаты реакций металлов с кислотами можно наблюдать?
При реакции металлов с кислотами можно наблюдать различные результаты. Некоторые металлы реагируют с кислотами интенсивно, выделяя водородный газ и образуя соли, например, цинк и соляная кислота. Другие металлы могут реагировать медленнее или вовсе не реагировать, например, золото и серебро обычно не реагируют с кислотами.
