Ортофосфорная кислота (H3PO4) является одним из наиболее распространенных неорганических кислот, используемых в промышленности и лабораторных условиях. Она имеет важное значение в химической промышленности, так как является исходным веществом для получения более сложных соединений фосфора.
При реакции с металлами ортофосфорная кислота проявляет свою кислотность и образует соли – ортофосфаты металлов. Однако не все металлы с ней реагируют. В основном, реактивность металлов с ортофосфорной кислотой зависит от их электрохимических свойств и их способности к окислению.
Некоторые металлы, такие как натрий (Na), калий (K), литий (Li) и магний (Mg), сильно реагируют с ортофосфорной кислотой. Они образуют соли с ортофосфорной кислотой и выделяются водородный газ (H2). При этой реакции их окислительная способность проявляется в том, что они окисляются до более высоких оксидов.
Однако более неподвижные и стабильные металлы, такие как железо (Fe), цинк (Zn), свинец (Pb) и серебро (Ag), не реагируют с ортофосфорной кислотой и не образуют с ней соли. Это связано с их низкой окислительной способностью и более слабой активностью по отношению к кислоте.
Металлы, взаимодействующие с ортофосфорной кислотой

Ортофосфорная кислота, также известная как фосфорная(V) кислота, представляет собой бинарное соединение фосфора и кислорода (H3PO4). Эта кислота является очень активным веществом и может взаимодействовать с различными металлами, образуя с ними соли - ортофосфаты.
Некоторые металлы, такие как натрий (Na), калий (K) и литий (Li), реагируют с ортофосфорной кислотой, образуя ортофосфаты металлов (например, Na3PO4). Эти ортофосфаты широко используются в различных отраслях промышленности, включая производство удобрений, стекла и металлургию.
Другие металлы, такие как железо (Fe), медь (Cu) и алюминий (Al), также проявляют реакцию с ортофосфорной кислотой. Они образуют соответствующие ортофосфаты металлов, которые могут быть использованы в различных промышленных процессах, включая производство лакокрасочных материалов и керамики.
Некоторые металлы, такие как серебро (Ag) и золото (Au), обычно не проявляют реакцию с ортофосфорной кислотой. Это связано с их высокой химической инертностью. Однако, в определенных условиях они все же могут образовывать ортофосфаты металлов.
Исходя из вышеизложенного, можно сделать вывод, что ортофосфорная кислота имеет широкий спектр реактивности с различными металлами. Это делает ее важным исходным материалом для производства различных продуктов и материалов в промышленности.
Алюминий, цинк и магний: химические свойства и признаки реакции с ортофосфорной кислотой

Алюминий:
Алюминий (Al) - это химический элемент, который обладает высокой реакционной способностью. При контакте с ортофосфорной кислотой (H3PO4), алюминий способен проявить реакцию, и образовать соль – алюминийфосфат (AlPO4). Реакция происходит следующим образом:
2Al + 3H3PO4 → Al2(PO4)3 + 3H2
При этом выделяется водород (H2), который можно наблюдать в виде газа.
Цинк:
Цинк (Zn) - это металл, который также реагирует с ортофосфорной кислотой. В результате этой реакции образуется цинково-фосфат (Zn3(PO4)2) и выделяется водород. Реакция выглядит следующим образом:
Zn + H3PO4 → Zn3(PO4)2 + H2
Подобно алюминию, цинк проявляет реакцию с ортофосфорной кислотой и выделяет водородный газ.
Магний:
Магний (Mg) - это легкий металл, который также может проявить реакцию с ортофосфорной кислотой. При взаимодействии магния с кислотой образуется магнийфосфат (Mg3(PO4)2) и выделяется водород. Реакция имеет вид:
Mg + 2H3PO4 → Mg3(PO4)2 + 3H2
Образование водорода является признаком происходящей реакции, и его можно наблюдать в виде газа.
Таким образом, алюминий, цинк и магний проявляют реакцию с ортофосфорной кислотой, образуя соответствующие фосфаты и выделяя водородный газ. Эти реакции можно использовать в химических исследованиях и промышленных процессах.
Железо, медь и свинец: особенности проявления реакции с ортофосфорной кислотой
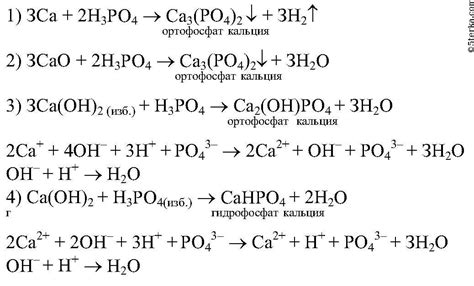
Ортофосфорная кислота, также известная как фосфорная кислота, является одной из наиболее распространенных и широко используемых кислот в химической промышленности. Она обладает высокой кислотностью и может проявлять реакцию с различными металлами, в том числе с железом, медью и свинцом.
Железо является одним из самых распространенных металлов, с которым может проявляться реакция ортофосфорной кислоты. При взаимодействии с кислотой железо образует соли ортофосфорной кислоты, которые имеют различные применения в промышленности и научных исследованиях.
Медь, в свою очередь, также может реагировать с ортофосфорной кислотой. Реакция меди с кислотой приводит к образованию солей, которые имеют важное значение в различных отраслях промышленности, включая электротехнику и строительство.
Свинец, как и железо и медь, проявляет реакцию с ортофосфорной кислотой. Кислота способна растворять свинцовые соединения, образуя соли, которые можно использовать в химическом производстве и других областях применения.
Никель, калий и натрий: взаимодействие с ортофосфорной кислотой и его применение в промышленности
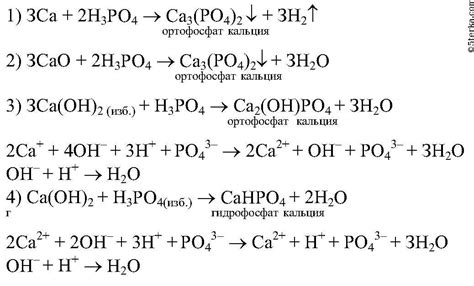
Ортофосфорная кислота, или H3PO4, является одной из наиболее широко используемых кислот в промышленности. Эта кислота проявляет реакцию с различными металлами, включая никель, калий и натрий. Взаимодействие этих металлов с ортофосфорной кислотой имеет свои особенности и применяется в различных отраслях промышленности.
Никель, как один из наиболее популярных металлов, проявляет реакцию с ортофосфорной кислотой. Данная реакция приводит к получению никелевого фосфата, который используется в производстве катализаторов, керамических материалов и других продуктов химической промышленности. Никелевый фосфат обладает высокой степенью термической стабильности и химической инертности, что делает его ценным материалом для различных технических приложений.
Калий и натрий также проявляют реакцию с ортофосфорной кислотой. В результате данной реакции образуются соответствующие фосфаты – калиевый фосфат (K3PO4) и натриевый фосфат (Na3PO4). Оба этих фосфата используются в производстве удобрений, поскольку они содержат в себе важные для растений питательные вещества: фосфор и калий (в случае с калиевым фосфатом) или фосфор и натрий (в случае с натриевым фосфатом). Эти фосфаты способствуют повышению урожайности и качества сельскохозяйственных культур.
Вопрос-ответ

Какие металлы реагируют с ортофосфорной кислотой?
Ортофосфорная кислота (H3PO4) обладает достаточно сильной кислотностью и может проявлять реакцию с различными металлами. К ним относятся, например, алюминий (Al), цинк (Zn), железо (Fe), никель (Ni), медь (Cu) и другие. Реакция с металлами проявляется в виде образования солей фосфорной кислоты и выделения водорода.
Есть ли какие-либо ограничения в реакции ортофосфорной кислоты с металлами?
Взаимодействие ортофосфорной кислоты с металлами может быть ограничено, например, активностью металла или степенью концентрации кислоты. Металлы, которые покрыты защитной пленкой оксида, такие как алюминий или магний, обычно менее активно реагируют с кислотой. Также степень реакции может зависеть от температуры, времени воздействия и других условий.
Что происходит при реакции ортофосфорной кислоты с металлами?
При реакции ортофосфорной кислоты с металлом происходит образование солей фосфорной кислоты и выделения водорода. Например, при взаимодействии кислоты с алюминием образуется алюминийфосфат и выделяется молекулярный водород. Реакция может протекать также с образованием кислорода или оксидов металла, в зависимости от условий реакции.
