Фтор - химический элемент с атомным номером 9 и обозначением F. Он относится к группе галогенов в периодической таблице, что делает его неметаллом. Фтор обладает рядом уникальных свойств, которые отличают его от других элементов.
Во-первых, фтор является самым электроотрицательным элементом в периодической таблице. Это означает, что он имеет большую способность притягивать электроны к себе. Эта особенность позволяет фтору образовывать сильные связи с другими элементами, что делает его идеальным для использования во многих химических соединениях.
Кроме того, фтор обладает высокой реактивностью. Он реагирует с большинством других элементов, образуя стабильные химические соединения. Фтор также обладает высокой термической и химической стойкостью, что делает его незаменимым во многих промышленных процессах и технологиях.
Фтор также обладает металлическими свойствами, что делает его уникальным среди неметаллов. Он имеет очень высокую электропроводность в жидком состоянии и высокую теплопроводность. Фтор также способен образовывать ионные соединения с металлами, обладая при этом высокой ионной мобильностью. Эта комбинация свойств делает фтор важным элементом во многих электронных и электротехнических приборах.
В заключении, фтор является химическим элементом, обладающим уникальными свойствами, которые делают его одним из самых важных элементов в нашей жизни. Он сочетает в себе особенности неметалла и металла, что позволяет использовать его в различных областях науки и промышленности.
Фтор как неметалл: его химические свойства и особенности

Фтор (F) - химический элемент с атомным номером 9 и атомной массой 18,9984032. Он относится к галогенам и является самым электронегативным элементом в периодической таблице. Фтор обладает рядом уникальных свойств, которые делают его неметаллом.
Одной из основных характеристик фтора является его высокая электроотрицательность. Этот элемент сильно притягивает электроны и проявляет высокую активность в химических реакциях. Фтор обладает высоким потенциалом окисления и образует соединения, такие как фториды, с большинством элементов в периодической таблице.
Еще одной особенностью фтора как неметалла является его способность образовывать ковалентные связи. Фтор обычно образует молекулы, в которых вокруг атома фтора находятся два электрона. Это делает его химические соединения стабильными и инертными.
Также стоит отметить, что фтор образует газообразный диатомный молекулярный фтор (F2), который является самым активным и реакционным состоянием этого элемента. Молекулярный фтор является сильным окислителем и способен взаимодействовать с множеством веществ.
В заключении, фтор - неметалл с высокой электроотрицательностью, способностью образовывать ковалентные связи и обладает высокой реакционностью. Его свойства делают его важным элементом во многих отраслях промышленности, таких как производство пластмасс, химическая аналитика и промышленность полупроводников.
Электроотрицательность и реактивность
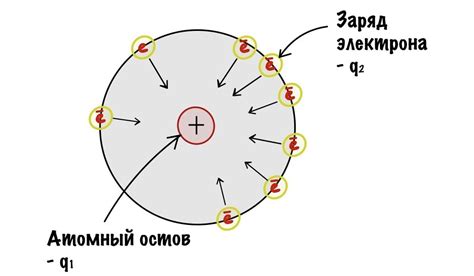
Электроотрицательность – это способность атома притягивать к себе электроны во время связывания с другими атомами. Фтор обладает самым высоким значением электроотрицательности среди всех химических элементов и, следовательно, проявляет выраженные кислотные свойства. Электроотрицательность фтора обусловлена его малым атомным радиусом и сильной заселенностью внешней электронной оболочки.
Реактивность фтора обусловлена его высокой электроотрицательностью и стремлением принять электроны, а также высокой энергией связи в молекулах фторида. Фтор считается самым реактивным химическим элементом и проявляет высокую агрессивность в реакциях с другими веществами.
Взаимодействуя с металлами, фтор образует металловолоконные соединения, такие как фториды. Они обладают высокой устойчивостью и полезны для различных промышленных процессов. Также фтор образует разнообразные органические соединения, которые находят применение в медицине, лакокрасочной промышленности и прочих отраслях. За счет своей высокой реактивности, фтор активно применяется в процессах фторирования, а также в процессе получения алюминия и других металлов.
Структура и физические свойства
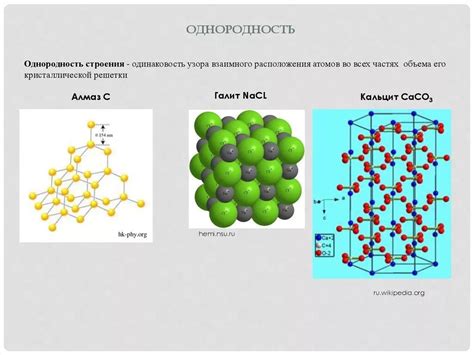
Фтор является неметаллом, обладающим характерными свойствами этой группы элементов. Он имеет атомный номер 9 и обозначается символом F. Структура атома фтора основана на электронной конфигурации 1s^22s^22p^5. Внешний электрон находится в p-подуровне, что делает его активным химическим элементом.
Одним из главных физических свойств фтора является его низкая температура плавления и кипения. При обычных условиях фтор находится в виде газа. Температура его кипения составляет -188.12 °C, а температура плавления -219.62 °C. Благодаря этим свойствам фтор часто используется в хладагентных системах для охлаждения и в качестве среды при низкотемпературных экспериментах.
Фтор обладает высокой реакционной способностью и активностью. Он образует соединения с большинством элементов и может вступать в химические реакции с различными веществами. Это свойство фтора делает его важным компонентом во многих процессах производства и применения различных химических соединений.
Одним из интересных физических свойств фтора является его способность к электроотрицательности. Фтор - самый электроотрицательный из всех химических элементов. Это означает, что он сильно притягивает электроны и обладает высокой способностью к образованию химических связей. Взаимодействие фтора с другими элементами позволяет создавать стабильные и прочные химические соединения.
Таким образом, структура и физические свойства фтора определяют его уникальные химические способности и широкое применение в различных отраслях промышленности и науки.
Применения фтора в различных отраслях промышленности

1. Производство алюминия
Фтор применяется для производства алюминия методом электролиза. В процессе электролиза фторид алюминия служит в качестве электролита, обеспечивая выделение металла.
2. Производство хлора и фтора
Фтор является сырьем для производства хлора и фтора, которые широко используются в промышленности. Фтор химически реагирует с логическим паром, образуя газообразный галоген в процессе фторации хлорида натрия.
3. Производство неорганических соединений
Фтор является необходимым компонентом при производстве многих неорганических соединений, таких как фториды, фосфаты и сульфаты. Эти соединения широко применяются в производстве стекла, керамики, а также в лабораторных условиях.
4. Производство фторированных органических соединений
Фтор используется при производстве фторированных органических соединений, таких как фторированные углеводороды и фторированные полимеры. Эти соединения обладают уникальными свойствами, такими как высокая термостабильность и устойчивость к химическим воздействиям.
5. Применение в электронике
Фтор используется в электронике для производства полупроводниковых материалов и покрытий. Фторированные соединения улучшают электрические и механические свойства материалов, что позволяет увеличить эффективность и надежность электронных устройств.
6. Применение в медицине
Фтор используется в медицине в качестве компонента зубной пасты и прополиса для профилактики кариеса. Он помогает укрепить зубную эмаль и предотвратить развитие зубного налета и кариеса.
7. Применение в огнезащитных материалах
Фторированные соединения используются в производстве огнезащитных материалов, таких как огнетушители и огнезащитные покрытия. Эти материалы помогают предотвратить распространение огня и защитить материалы от высоких температур.
Вопрос-ответ

Какие свойства характерны для фтора как неметалла?
У фтора есть ряд свойств, характерных для неметаллов. Например, он имеет низкую температуру плавления и кипения, ярко выраженную электроотрицательность, ионизационную энергию и энергию атомного радиуса. Фтор обладает высокой активностью и реактивностью, способностью образовывать ковалентные и ионные соединения, а также кислотную окислительную способность.
Чему обязано присутствие металлоподобных свойств у фтора?
Присутствие металлоподобных свойств у фтора обусловлено его высокой электроотрицательностью и малым радиусом атома. Из-за высокой электроотрицательности фтор обладает способностью принимать электроны и образовывать отрицательные ионы. В то же время, благодаря своему малому атомному радиусу, фтор может образовывать металлоподобные катионы и обладать металлическими свойствами, такими как теплопроводность и электропроводность.
Какие еще особенности химического элемента фтора можно выделить?
Особенности химического элемента фтора включают высокие окислительные свойства, специфическую химическую активность и связанную с ней опасность. Фтор обладает необычайно высокой электроотрицательностью и способен образовывать сложные соединения с другими элементами. Кроме того, фтор является очень реактивным элементом и может вступать во множество химических реакций, часто сопровождающихся выделением тепла или света.
