Концентрированная серная кислота является одним из самых распространенных и важных химических реагентов. Она обладает множеством применений в различных отраслях промышленности, лабораторной практике и повседневной жизни. Одной из интересных реакций, которые могут происходить с участием серной кислоты, является ее взаимодействие с металлами.
Под действием концентрированной серной кислоты некоторые металлы проявляют активность и начинают выделять газы. Это связано с реакцией металла с кислотой, в результате которой образуются соли соответствующих металлов и выделяется водородный газ. Водород является легким и горючим газом, поэтому его образование и выделение при реакции с серной кислотой может сопровождаться появлением пламени.
Реакция концентрированной серной кислоты с металлами основана на окислении металла и одновременном восстановлении кислоты, что приводит к образованию солей и выделению водорода.
Такая реакция может проходить со многими металлами, но не с каждым. Некоторые металлы, такие как алюминий, цинк, железо и медь, проявляют активность и способны реагировать с серной кислотой, тогда как другие металлы, например, свинец и золото, эту реакцию не проходят. Для проведения такой реакции требуется концентрированная серная кислота, поскольку только она обладает достаточной активностью и агрессивностью для окисления металлов.
Что происходит при реакции металлов с серной кислотой?

При реакции металлов с концентрированной серной кислотой происходит выделение газа в виде сероводорода (H2S). Металлы активной группы, такие как цинк (Zn), железо (Fe) или алюминий (Al), реагируют с серной кислотой, образуя соответствующие соли и высвобождая сероводород.
Реакция металлов с серной кислотой происходит по следующей схеме: металл вступает в реакцию с серной кислотой, образуя соль металла и воду. При этом одним из побочных продуктов образуется сероводородный газ.
Реактивность металлов, проявляющаяся при их взаимодействии с серной кислотой, зависит от их электрохимического потенциала. Металлы с более низкими значениями потенциала (активные металлы) реагируют с серной кислотой более активно, выделяя больше сероводорода. При этом активные металлы вступают в реакцию с серной кислотой довольно быстро и образуют соли, в то время как менее активные металлы могут реагировать медленнее и давать менее интенсивное выделение газа.
Выделение сероводорода во время реакции может быть обнаружено с помощью химического датчика или по характерному запаху газа, который имеет запах гнилого яйца. Процесс выделения сероводорода является одной из характерных особенностей реакции металлов с серной кислотой.
Выбор металла для проведения реакции
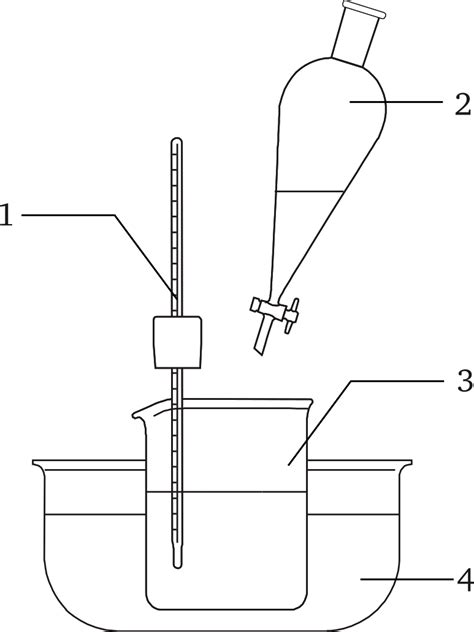
При проведении реакции концентрированной серной кислоты с металлами необходимо правильно выбрать металл, чтобы получить выделение газа исключительно желаемого вида.
Одним из важных факторов, влияющих на выбор металла, является его активность. Активность металлов определяется их способностью взаимодействовать с кислотами. Наиболее активные металлы, такие как натрий, калий или литий, реагируют с серной кислотой быстро и интенсивно, при этом выделяется большое количество газа.
Другим важным фактором для выбора металла является его стоимость и доступность. Некоторые металлы могут быть более дорогими или редкими, что делает их нецелесообразными для использования в данной реакции. Поэтому часто выбирают более дешевые и широко доступные металлы, такие как цинк, железо или алюминий.
Также необходимо учитывать свойства металла, такие как его химическая стабильность и реакционная способность. Некоторые металлы могут образовывать стабильные оксиды или гидроксиды, которые могут затруднить реакцию с серной кислотой.
Подытоживая, выбор металла для проведения реакции зависит от его активности, доступности и стоимости, а также от свойств металла, которые могут повлиять на протекание реакции и выделение газа.
Как происходит реакция?

Реакция концентрированной серной кислоты с металлами – это пример распада кислоты. При этом образуется газ, который, в зависимости от металла, может быть взрывоопасным, горючим или безвредным.
Для начала реакции необходимо подготовить металлический образец и сосуд для проведения эксперимента. Металл помещается в сосуд, после чего добавляется концентрированная серная кислота. В процессе реакции металл общается с кислотой, при этом происходит окисление металла и восстановление кислоты.
В результате взаимодействия металла и кислоты выделяется газ и образуется раствор соли соответствующего металла. Газ может накапливаться в сосуде или выводиться через специальную аппаратуру для его накопления или измерения. При некоторых реакциях, например с цинком, в результате выделения газа возникает пена или бурлящий поток.
Степень интенсивности реакции зависит от концентрации кислоты и природы металла. Некоторые металлы реагируют с серной кислотой спонтанно и с большим выделением газа, в то время как другие, такие как железо или свинец, могут реагировать медленно. Важно также учитывать, что эта реакция происходит с выделением тепла и осуществляется в закрытой системе.
Какие газы выделяются при реакции?

При реакции концентрированной серной кислоты с металлами могут выделяться различные газы в зависимости от выбранного металла. Это связано с тем, что серная кислота может взаимодействовать с разными металлами, образуя различные продукты реакции.
Взаимодействие серной кислоты с щелочными металлами, такими как натрий (Na), калий (K) или литий (Li), приводит к выделению водорода (H2) в виде газа. Это связано с тем, что щелочные металлы реагируют с серной кислотой, образуя соли и освобождая молекулы водорода.
С другими металлами, такими как цинк (Zn), железо (Fe) или алюминий (Al), серная кислота реагирует с образованием газовых продуктов, таких как диоксид серы (SO2) или диоксид углерода (CO2). Данные газы образуются в результате окисления металла серной кислотой и могут иметь характерный запах и цвет.
Также возможна реакция серной кислоты с неметаллами, например, смесью угольной пыли и серы, где также выделяется диоксид серы. В этом случае, воздействие серной кислоты на неметаллические компоненты приводит к образованию продуктов с различной степенью окисления серы.
Применение газа, выделяющегося при реакции
Газ, выделяющийся при реакции концентрированной серной кислоты с металлами, имеет широкое применение в различных областях. Он обладает рядом полезных свойств, что делает его ценным ресурсом для промышленности и научных исследований.
Прежде всего, выделяющийся газ может быть использован в качестве источника энергии. Он может быть сжатым и использован для питания двигателей и генераторов. Таким образом, газ может быть использован как альтернативный источник энергии, что позволяет сократить использование ископаемых топлив и сократить вредные выбросы в атмосферу.
Кроме того, газ имеет высокую окислительную способность, что позволяет его использовать в процессах окисления исходных веществ. Он может быть применен в химическом производстве для получения различных химических соединений, включая кислоты, основания и соли. Благодаря своей окислительной способности, газ также может быть использован в качестве реактивного вещества при получении различных соединений с использованием органических веществ.
Важным применением газа, выделяющегося при реакции, является его использование в аналитических методах. Газ может быть использован в химическом анализе для определения наличия определенных элементов или соединений. Также он может быть использован для определения концентрации веществ, так как реакция с газом происходит в избытке и учитывается количество выделившегося газа.
Другим важным применением газа является его использование в медицине и фармацевтике. Он может быть использован для проведения стерилизации медицинских инструментов и материалов, так как он обладает антимикробными свойствами. Также газ может использоваться в процессе синтеза лекарственных препаратов, так как его реактивные свойства позволяют проводить химические преобразования для получения нужных соединений.
Особенности реакции при использовании разных металлов

Реакция концентрированной серной кислоты с металлами может протекать по-разному в зависимости от химических свойств и активности металла. При взаимодействии серной кислоты с разными металлами возможны различные характеристики реакции.
Металлы с низкой электрохимической активностью, такие как золото и платина, реагируют с серной кислотой очень медленно или практически не реагируют в обычных условиях. Это связано с тем, что такие металлы обладают высокой устойчивостью к коррозии и слабо взаимодействуют с окислителем – серной кислотой.
Металлы средней активности, такие как железо, медь, цинк и свинец, при взаимодействии с серной кислотой образуют соответствующие соли металлов и выделяются обычно водород. Реакция средней активности проходит достаточно интенсивно и может сопровождаться выделением тепла и пенообразованием.
Активные металлы, такие как натрий, калий, алюминий и магний, проявляют особенно высокую реактивность при взаимодействии с серной кислотой. В результате такой реакции образуется сернистый газ (диоксид серы), который видится в виде белых паров или дыма. Реакция с активными металлами может сопровождаться ожогами и мгновенным выделением большого количества тепла.
Безопасность при проведении реакции

При проведении реакции концентрированной серной кислоты с металлами необходимо соблюдать определенные меры безопасности, чтобы предотвратить возможные аварийные ситуации и защитить здоровье людей.
Во-первых, необходимо работать в хорошо проветриваемом помещении или под вытяжкой, чтобы избежать ингаляции опасных газов. Также рекомендуется использовать средства индивидуальной защиты, такие как защитные очки, резиновые перчатки и халат.
При добавлении металлов в кислоту нужно быть осторожным, чтобы избежать брызг серной кислоты, которые могут вызвать химические ожоги на коже и глазах. Рекомендуется использовать специальное оборудование для добавления реагентов.
Следует помнить, что при этой реакции выделяется водородный газ, который является горючим. Поэтому необходимо держаться подальше от источников открытого огня, не курить и не использовать электрооборудование вблизи места проведения реакции. Также не рекомендуется проводить реакцию вблизи легко воспламеняющихся веществ.
Важно также помнить о правильной утилизации полученных реакционных продуктов. Водородный газ должен быть аккуратно выброшен или сожжен в безопасных условиях. Остатки серной кислоты и других веществ должны быть изолированы и утилизированы в соответствии со специальными требованиями и нормами.
Все эти меры безопасности необходимо соблюдать, чтобы минимизировать возможные риски при проведении реакции концентрированной серной кислоты с металлами и обеспечить безопасность как самих исполнителей, так и окружающей среды.
Вопрос-ответ

Какой газ выделяется при реакции концентрированной серной кислоты с металлами?
При реакции концентрированной серной кислоты с металлами образуется водородный газ (H2).
Какие металлы реагируют с концентрированной серной кислотой и выделяют газ?
Взаимодействие концентрированной серной кислоты с металлами протекает только при наличии более активного металла, чем водород. Например, цинк (Zn), железо (Fe), алюминий (Al) и свинец (Pb) реагируют с концентрированной серной кислотой, образуя водородный газ.
Почему происходит выделение газа при реакции концентрированной серной кислоты с металлами?
При взаимодействии концентрированной серной кислоты с металлами происходит реакция окисления и восстановления. Кислота (H2SO4) отдаёт свои протоны металлу, образуя соль и выделяя водородный газ. Это обусловлено тем, что металлы имеют большую аффинность к кислороду, чем кислород воды (H2O), поэтому они отбирают у серной кислоты протоны, образуя водород.
