Галогениды металлов представляют собой комплексы, образованные соединениями металла с галогеном – хлором, фтором, бромом или йодом. Эти соединения обладают уникальными химическими свойствами и находят широкое применение в различных областях науки и промышленности.
Одной из особенностей галогенидов металлов является их высокая химическая реактивность. Галогениды металлов обладают сильными окислительными свойствами, что позволяет использовать их в качестве окислителей в различных химических реакциях. Кроме того, галогениды металлов могут образовывать стабильные комплексы с органическими соединениями, что делает их важными ингредиентами при синтезе органических соединений.
Применение галогенидов металлов обширно в различных областях науки и промышленности. Например, они активно используются в химической промышленности при производстве пластмасс, красителей, фармацевтических препаратов и других продуктов. Они также применяются в процессе химического анализа для выделения и идентификации различных веществ. Кроме того, галогениды металлов находят применение в электронике и электротехнике, например, в качестве компонентов электролитов и электролюминесцентных материалов.
Галогениды металлов: свойства и применение
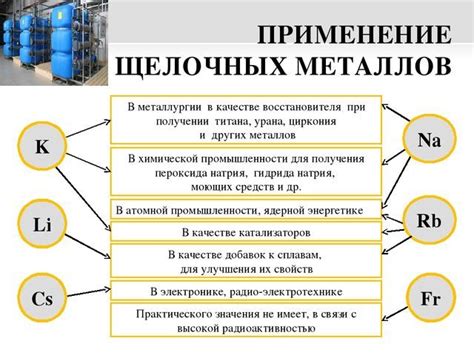
Галогениды металлов – это соединения, образующиеся при сочетании одного или нескольких галогенов (фтора, хлора, брома, йода) с металлами. Они обладают рядом особых свойств, которые находят применение как в научных исследованиях, так и в разных технологических процессах.
Главной характеристикой галогенидов металлов является их высокая степень растворимости в различных растворителях. Благодаря этому свойству, галогениды металлов нашли применение в различных процессах, включая электролиз, осаждение металлов на поверхности и получение материалов с заданными свойствами.
Один из выдающихся примеров применения галогенидов металлов – это использование йодидов в медицине. Иод является неотъемлемым компонентом многих важных медицинских препаратов. Он используется для лечения различных заболеваний щитовидной железы, а также в процессах стерилизации.
Галогениды металлов также широко применяются в различных областях науки. Например, хлорид железа используется в качестве катализатора в химических реакциях. Фториды металлов применяются в области полупроводниковой технологии для создания высокоэффективных и надежных полупроводниковых устройств.
В заключение можно отметить, что свойства и применение галогенидов металлов сильно варьируются в зависимости от конкретных соединений и металлов, с которыми они сочетаются. Использование галогенидов металлов в различных процессах и областях позволяет получать новые материалы с уникальными свойствами и улучшать существующие технологии.
Обзор химических свойств галогенидов металлов
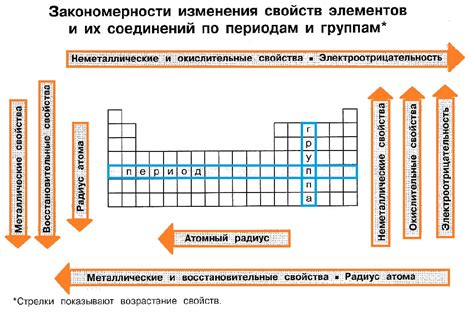
Галогениды металлов представляют собой соединения, состоящие из галогенов и металлов. В зависимости от типа галогена, химические свойства галогенидов металлов могут значительно варьироваться.
Галогениды металлов обладают различными физическими и химическими свойствами. Одним из основных свойств галогенидов металлов является их тугоплавкость. Некоторые галогениды металлов обладают высокой температурой плавления и кипения, что делает их ценными для использования в высокотемпературных процессах.
Галогениды металлов также обладают высокой растворимостью в воде, что позволяет использовать их в химическом анализе и в процессах синтеза различных соединений. Они могут служить катализаторами различных химических реакций.
Некоторые галогениды металлов обладают ярко выраженными свойствами флуоресценции, что находит применение в оптике и электронике. Они также могут использоваться в процессе создания люминесцентных материалов и фосфоров.
Галогениды металлов играют важную роль в различных отраслях промышленности и науки. Они используются в производстве лекарственных препаратов, керамики, лакокрасочных материалов, полупроводников и других продуктов. Благодаря своим уникальным химическим свойствам, галогениды металлов становятся все более востребованными и находят широкое применение в различных областях науки и технологий.
Особенности галогенидов металлов при взаимодействии с растворами

Галогениды металлов – это соединения, состоящие из металлического катиона и аниона галогена. При взаимодействии с растворами, галогениды металлов обладают рядом особенностей.
Растворимость: В целом, галогениды металлов хорошо растворяются в воде. Однако, растворимость может различаться в зависимости от конкретного галогенида и металла.
Гидролиз: Значительное количество галогенидов металлов образуют кислые растворы из-за гидролиза. Гидролиз – это реакция с водой, при которой образуются ион гидроксида и кислота. Из-за этого, растворы галогенидов металлов могут быть коррозионно-активными и оказывать влияние на окружающую среду.
Ионизация: В растворе галогениды металлов могут ионизироваться, образуя отрицательно заряженные анионы галогенов и положительно заряженные катионы металлов. Это позволяет использовать галогениды металлов в качестве электролитов.
Применение: Галогениды металлов широко используются в различных областях промышленности и науки. В качестве примера можно привести использование хлорида натрия (NaCl) в пищевой промышленности, где он используется как добавка для придания пикантности и солоноватого вкуса продуктам.
Таким образом, галогениды металлов обладают своими особенностями при взаимодействии с растворами, что делает их важными и широко применимыми соединениями в различных областях.
Применение галогенидов металлов в промышленности

Галогениды металлов – это соединения, в которых металл связан с атомами галогенов (фтора, хлора, брома, йода). Эти соединения широко используются в различных отраслях промышленности благодаря своим уникальным химическим свойствам.
Одним из важных применений галогенидов металлов является их использование в процессах металлургии. Например, хлорид натрия (NaCl) применяется в процессе получения алюминия методом электролиза. Использование галогенидов металлов в этих процессах позволяет улучшить их эффективность и снизить затраты на производство.
Галогениды металлов также находят применение в производстве керамических материалов. Например, фторид кальция (CaF2) добавляется в стекломассу для повышения ее термической стойкости. Бромид меди (CuBr) используется в процессе обработки поверхности керамических изделий, благодаря чему достигается улучшение их эстетических свойств.
Галогениды металлов также находят применение в производстве электроники. Например, хлорид магния (MgCl2) используется для создания пленок, которые применяются в процессе изготовления полупроводниковых элементов. Эти пленки обеспечивают необходимую электропроводность и защиту от внешних воздействий.
Кроме того, галогениды металлов используются в процессе производства лакокрасочных материалов. Например, хлорид цинка (ZnCl2) применяется в качестве катализатора при получении пластиковых красок. Это позволяет улучшить стойкость краски к внешним воздействиям и повысить ее срок службы.
Таким образом, галогениды металлов играют важную роль в различных отраслях промышленности, обеспечивая улучшение качества и эффективности производимых материалов и изделий.
Перспективные направления использования галогенидов металлов в науке и технологиях

1. В качестве катализаторов
Галогениды металлов представляют собой эффективные катализаторы для различных химических реакций. Они могут ускорять протекание реакций, снижать энергию активации и улучшать выход продукта. Применение галогенидов металлов в качестве катализаторов может быть использовано в процессах синтеза органических соединений, окислительных процессах, а также в производстве полимеров.
2. В электрохимии
Галогениды металлов обладают интересными электрохимическими свойствами, что делает их полезными материалами для создания электродов, батарей и других устройств, использующих электрохимические процессы. Например, галогениды металлов могут быть использованы в производстве аккумуляторов с высокой энергетической плотностью или в суперконденсаторах с высокой емкостью.
3. В фотонике
Галогениды металлов обладают уникальными оптическими свойствами, что делает их применение в фотонике особенно интересным. Они могут использоваться в качестве материалов для создания оптических волокон, лазеров и других устройств, работающих на основе взаимодействия света с веществом. Применение галогенидов металлов в фотонике может привести к созданию более эффективных и мощных оптических устройств.
4. В материаловедении
Галогениды металлов являются важными материалами в материаловедении благодаря своим уникальным физическим свойствам. Они могут быть использованы для создания магнитных материалов, полупроводников, материалов с определенными оптическими свойствами и других материалов с заданными характеристиками.
5. В медицине
Галогениды металлов также находят применение в медицине. Они могут быть использованы в качестве противоопухолевых препаратов, антисептиков, антибиотиков и обладать другими полезными медицинскими свойствами. Исследования в данном направлении могут привести к созданию новых эффективных препаратов и методов лечения различных заболеваний.
Вопрос-ответ

Какие химические свойства имеют галогениды металлов?
Галогениды металлов обладают свойствами, свойственными как металлам, так и галогенам. Они хорошо растворяются в воде и образуют ионные соединения. Кроме того, галогениды металлов обладают высокой реакционной способностью из-за наличия активного галогена в своем составе.
Какие особенности есть у галогенидов металлов?
Особенностью галогенидов металлов является их способность образовывать структурные и цветовые модификации. Это связано с особенностями строения и взаимодействия атомов галогена и металла. Кроме того, галогениды металлов могут иметь различные степени окисления металла, что также влияет на их свойства.
Какие галогениды металлов наиболее распространены?
Наиболее распространены галогениды металлов, содержащие хлор, бром и йод. Например, хлорид натрия (NaCl), бромид железа (FeBr2) и йодид калия (KI).
Какие применения имеют галогениды металлов?
Галогениды металлов имеют широкое применение в различных областях. Например, хлорид натрия используется в пищевой промышленности для приготовления пищевых добавок, бромид железа применяется в медицине для лечения некоторых заболеваний, а йодид калия используется в фотографии для приготовления эмульсии.
Какие свойства галогенидов металлов делают их полезными в различных процессах?
Среди свойств галогенидов металлов, которые делают их полезными в различных процессах, можно выделить их высокую растворимость, высокую устойчивость при высоких температурах и возможность образования структурных модификаций. Благодаря этим свойствам галогениды металлов находят применение в химической промышленности, медицине, фотографии и других отраслях.
