Электроны - основные частицы, определяющие химические свойства атомов. Понимание того, сколько электронов содержит атом, играет важную роль в химии и физике. Общее число электронов в атоме зависит от нескольких факторов, которые нужно рассмотреть в контексте структуры атома.
Рассмотрим первый фактор - структура атома. Каждый атом состоит из ядра, содержащего протоны и нейтроны, и облака электронов, которые находятся на разных энергетических уровнях. Каждый энергетический уровень может содержать определенное количество электронов, что определяет общее число электронов в атоме.
Второй фактор - электронная конфигурация. Электроны в атоме распределены по энергетическим уровням и подуровням, что определяет их взаимодействие. Электронная конфигурация каждого элемента позволяет определить, сколько электронов он содержит и как они распределены по орбиталям.
Физические факторы влияющие на число электронов в атоме
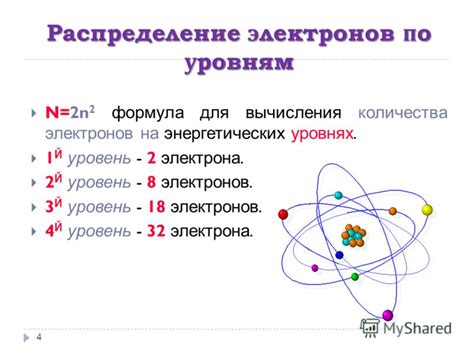
В атоме число электронов определяется несколькими физическими факторами, включая:
| 1. Заряд ядра | Чем больше заряд ядра, тем больше электронов может удерживать в себе атом. |
| 2. Энергетические уровни | Каждый атом имеет определенное количество энергетических уровней, на которых могут находиться электроны. Каждый уровень может вмещать определенное количество электронов. |
| 3. Уровни заполнения электронов | Существуют правила заполнения электронами энергетических уровней, например, принцип Паули, принцип Гунда и принцип Гейзенберга, что также влияет на общее число электронов в атоме. |
Влияние ядерного заряда на количество электронов
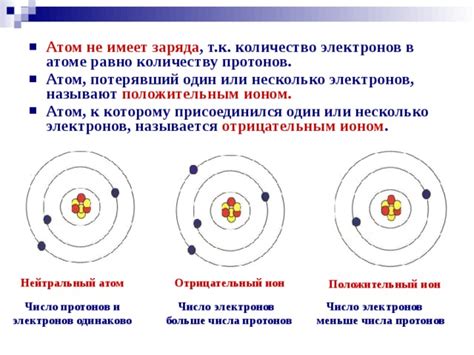
Количество электронов в атоме тесно связано с ядерным зарядом. Ядерный заряд определяет количество протонов в ядре атома, что, в свою очередь, определяет его химические свойства и положение в периодической таблице элементов.
Согласно закону Кулона, чем больше ядерный заряд, тем сильнее он притягивает к себе электроны. Это означает, что атомы с большим ядерным зарядом имеют большее количество электронов в своих оболочках, поскольку электроны остаются ближе к ядру.
Таким образом, число электронов в атоме в значительной степени зависит от ядерного заряда и определяется химическими свойствами элемента.
Роль квантовых законов в определении числа электронов

Число электронов в атоме определяется квантовыми законами, которые учитывают энергетические уровни электронов и запрет на наличие электронов с одинаковыми квантовыми числами.
Принцип заполнения энергетических уровней: В соответствии с принципом Паули ни один электрон не может иметь одинаковые все четыре квантовые числа с другим электроном.
Специфика заполнения электронных оболочек атома связана с квантовыми числами, определяющими энергетические состояния электронов и их распределение по орбиталям.
Электронные оболочки как основной параметр определения числа электронов
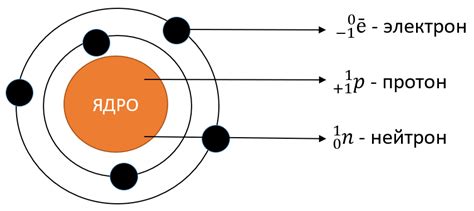
Правило Хунда утверждает, что электроны заполняют орбитали отдельно и сначала с темперты орбиталей минимальной энергии.
Таким образом, зная количество электронов в последней оболочке атома, можно определить его химические свойства и взаимодействия с другими элементами.
Вопрос-ответ

Чем определяется общее число электронов в атоме?
Общее число электронов в атоме определяется зарядом ядра атома, который равен числу протонов. По своей природе атомы стремятся быть электрически нейтральными, поэтому количество электронов равно количеству протонов в ядре. Это число представляется атомным номером, который однозначно идентифицирует каждый химический элемент в периодической системе.
Каковы основные факторы, влияющие на количество электронов в атоме?
Основные факторы, определяющие количество электронов в атоме, включают атомный номер элемента, его электронную конфигурацию, а также его химические свойства. Атомный номер определяет количество протонов и, следовательно, электронов в атоме. Электронная конфигурация описывает распределение электронов по энергетическим уровням и субуровням вокруг ядра.