Эквивалентное число вещества (экв.) - это количество вещества, которое содержит определенное количество зарядов.
Для рассчета эквивалентного числа вещества CaCO3 необходимо учитывать молярную массу вещества и количество ионов, которые способно отдать или принять вещество.
В данной статье мы рассмотрим методику расчета эквивалентного числа вещества CaCO3 и дадим примеры применения данного понятия в химических реакциях.
Способы определения

Другой метод – гравиметрическое определение, основанное на осаждении преципитата, затем его фильтрации, промывке и высушивании для определения массы и тем самым расчета содержания эквивалентного числа вещества.
Измерение объема газа

Для рассчета эквивалентного числа вещества CaCO3 необходимо провести измерение объема газа, который выделяется при реакции с образованием осадка. Для этого применяют специальные приборы, такие как газообразователи или газовые сборники. Объем газа измеряется в миллилитрах (мл) с помощью градуированных колб или бюреток.
Важно учитывать, что при измерении объема газа необходимо учитывать стандартные условия (нормальные условия температуры и давления), чтобы исправить объем газа до стандартных условий и получить точные данные.
Масса вещества на основе реакции
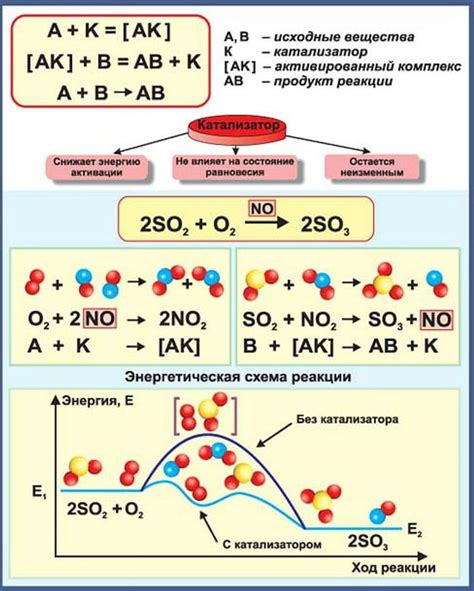
Для расчета эквивалентного числа вещества CaCO3 необходимо знать массу источника кальция (Ca) и массу углерода (C) в соединении. Процедура вычисления включает в себя определение массовой доли кальция и углерода в образце, а затем преобразование их в количество вещества.
Известная масса кальция (Ca) и масса углерода (C) могут быть использованы для расчета эквивалентного числа вещества CaCO3, которое будет эквивалентно им в реакции. Этот метод позволяет оценить количество CaCO3, необходимое для получения тех же показателей кальция и углерода, что и в изначальном образце.
Используя рассчитанное эквивалентное число вещества CaCO3, можно установить соотношение между массой исходного образца и необходимым количеством CaCO3, что облегчает понимание химических превращений и позволяет оптимизировать процессы получения соединений кальция.
Практическое применение

В аналитической химии

Рассчет эквивалентного числа вещества CaCO3 важен для определения содержания кальция в образцах. Для этого необходимо провести титрование образца раствором хлорной кислоты с использованием индикатора. После титрования можно рассчитать эквивалентное число вещества CaCO3 по формуле:
| Объем титранта, мл | Нормальность титранта, Н |
|---|---|
| V | N |
Эквивалентное число вещества CaCO3 вычисляется по формуле: E(CaCO3) = V * N / 2, где V - объем титранта, а N - нормальность титранта. Полученное значение можно использовать для расчета содержания кальция в исследуемом образце.
Применение в производстве

Эквивалентное число вещества CaCO3 широко используется в различных отраслях промышленности:
- В пищевой промышленности для регулирования рН и улучшения текстуры продуктов
- В строительстве для изготовления строительных материалов, таких как известковый штукатурка и краска
- В химической промышленности для обработки воды, очистки газов и производства химических соединений
- В фармацевтике для производства лекарственных препаратов
Это важный параметр, который помогает контролировать процессы и обеспечивать качество производимых продуктов.
Вопрос-ответ

Как рассчитать эквивалентное число вещества CaCO3?
Для этого необходимо умножить массу исходного вещества на его молярную массу и затем поделить на молярную массу CaCO3. Таким образом, получится эквивалентное число вещества CaCO3.
Зачем нужно вычислять эквивалентное число вещества CaCO3?
Расчет эквивалентного числа вещества CaCO3 позволяет сравнивать разные вещества по их воздействию на окружающую среду или процессы в химических реакциях.
Какой смысл в использовании эквивалентного числа вещества CaCO3?
Эквивалентное число вещества CaCO3 позволяет стандартизировать и сравнивать различные химические реакции и процессы в отношении их воздействия и взаимодействия с окружающей средой.