Существует удивительный мир, в котором все ларчики открываются очень просто - достаточно только немного поднять температуру, и все становится совсем иначе. Процесс плавления и изменения температуры - это фундаментальные законы, лежащие в основе множества физических и химических явлений. Подобно танцу капелек воды на раскаленной сковороде, проникновению зимнего мороза в костры сухой древесины или смене агрегатного состояния обычной жидкости в результате нагрева - все это - фасады великого спектра изменений, где каждый фактор играет свою роль, помогая нам понять, как работает мир веществ.
Давайте окунемся в мир термических явлений и узнаем, какая взаимосвязь существует между изменением температуры и различными элементами вещества. Открытие двери в невероятную внутреннюю жизнь материи начинается с проникновения наших мыслей за пределы обычных определений. Каждый факт, каждое явление имеет глубинные корни, и чтобы понять их, нам необходимо узреть эти связи, почувствовать потоки энергии и увидеть невидимое взаимодействие.
Когда замерзает вода, мы видим, как тонкие льдинки образуют на поверхности тонкую пленку, а затем весь поток становится твёрдым и ломким. Что происходит с молекулами вещества, когда они претерпевают изменение температуры? Для понимания этого нам придется пристально изучить основные законы термодинамики, где мир веществ находится в постоянном движении и изменении. Каждая молекула, каждая частица вещества - это своего рода микромир, где живут свои законы и своя внутренняя динамика.
Взаимосвязь температуры и изменение состояния вещества
Температура играет крайне важную роль в определении фазовых переходов, через которые проходят вещества. Эти переходы включают в себя не только плавление и кипение, но и конденсацию, замерзание, сублимацию и ряд других процессов.
Истинная сущность фазовых переходов кроется в изменении микроструктуры вещества, и температура является главной переменной, которая запускает эти изменения. Воздействуя на атомы, молекулы и ионы, повышение или понижение температуры приводит к изменению их движения и взаимодействия, что в конечном итоге приводит к изменению физических свойств вещества.
При повышении температуры, когда энергия движения частиц становится достаточно большой, связи между частицами начинают ослабевать. Это может вызвать разрушение упорядоченной структуры вещества и привести к переходу от твердого состояния к жидкому. Этот процесс называется плавлением.
Наоборот, понижение температуры может воздействовать на движение частиц, снова укрепляя связи между ними. Это может привести к формированию регулярной опорядоченной сетки и переходу от жидкого состояния к твердому. Этот процесс называется замерзанием.
Температура также определяет условия сублимации, когда вещество переходит непосредственно из твердого состояния в газообразное, и обратного процесса - конденсации, когда газообразное вещество переходит в твердое состояние без промежуточного жидкого этапа.
Таким образом, понимание взаимосвязи между температурой и фазовыми переходами позволяет нам лучше осознать, как изменения температуры влияют на состояние вещества и его свойства. Это имеет важное значение во многих практических областях, от производства материалов до понимания основных принципов физической и химической термодинамики.
Роль теплоты в процессах плавления и замерзания
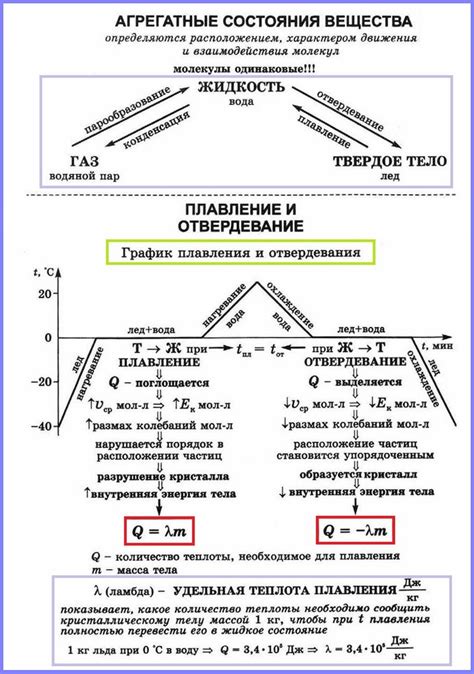
Теплота, также известная как термическая энергия, представляет собой форму энергии, связанную с движением атомов и молекул вещества. Она может передаваться от одного объекта к другому и способна вызвать изменение его состояния.
В процессе плавления теплота играет роль "разрушителя" структуры вещества. Под воздействием высоких температур, теплота позволяет атомам и молекулам приобретать достаточную энергию для преодоления сил взаимодействия и "освобождения" из их упорядоченных образований. Таким образом, твердое тело становится жидким.
В случае замерзания происходит обратный процесс. Путем отвода теплоты от жидкости к окружающей среде, атомы и молекулы медленно упорядочиваются, образуя регулярную решетку. Это приводит к образованию твердого тела, где частицы уже не свободно перемещаются, а занимают фиксированные позиции.
Таким образом, теплота является определяющим фактором в процессах плавления и замерзания. Более высокие температуры способствуют плавлению, позволяя частицам совершать больше хаотических движений и нарушать упорядоченность их расположения. Наоборот, отвод теплоты вызывает замерзание, когда атомы и молекулы упорядочиваются, образуя твердое тело.
Влияние температуры плавления на свойства веществ

Рассмотрим, как температура, при которой вещество начинает плавиться, влияет на его характеристики и свойства.
Одно из основных свойств, зависящих от температуры плавления, - это фазовый переход вещества из твердого состояния в жидкое. При достижении определенной температуры, которая может варьироваться от вещества к веществу, происходит разрушение кристаллической решетки и переход атомов или молекул в более подвижное состояние. Это приводит к образованию молекулярных или ионных связей, обеспечивающих поддержание жидкого состояния.
Степень подвижности извлекаемых атомов или молекул влияет на другие свойства вещества, такие как вязкость, поверхностное натяжение и теплопроводность. С увеличением температуры плавления, подвижность частиц увеличивается, и, следовательно, вязкость вещества уменьшается. Это может быть важным при выборе материала для специфических приложений, например, в машиностроении или химической промышленности.
Температурные изменения влияют также на поверхностное натяжение вещества. С повышением температуры плавления, силы притяжения между молекулами снижаются, и поверхностное натяжение уменьшается. Это может привести к изменению всплеска жидкости, а также к более легкому проникновению жидкости в пористые материалы.
Кроме того, температура плавления оказывает влияние на теплопроводность вещества. С повышением температуры, энергия кинетического движения молекул возрастает, что способствует более эффективному переносу тепла через вещество. Это может быть полезным при разработке материалов для использования в высокотемпературных условиях, таких как теплообменники или плавильные печи.
Неопределенность Гейзенберга и воздействие на термодинамику

Неопределенность Гейзенберга может иметь важные последствия для понимания взаимодействия между физическими системами и изменения температуры. Когда мы измеряем физическую систему, например, измеряем ее температуру, мы воздействуем на нее и видим только усредненные результаты. Ограничение неопределенности приводит к тому, что мы не можем одновременно измерить точное положение тела и его импульс, а следовательно, и точную температуру, которая связана с движением частиц.
Таким образом, неопределенность Гейзенберга оказывает определенное влияние на наши знания о изменении температуры. Взаимодействие между измеряемой системой и измерительным прибором создает неопределенность, которая накладывает ограничения на нашу возможность точного измерения и понимания термодинамических процессов.
Взаимосвязь между квантовой механикой и процессом плавления вещества

Рассмотрение явления плавления вещества с позиции квантовой механики позволяет раскрыть новые аспекты исследования этого процесса. Квантовый подход привносит в общую картину новые закономерности, связывающие потерю твердой структуры вещества с квантовыми состояниями его атомов и молекул.
Один из ключевых факторов, определяющих изменение свойств вещества при плавлении, является изменение энергетического состояния его частиц. В квантовой механике эти состояния выражаются через кванты энергии, каждый из которых соответствует конкретному значению энергии. Плавление происходит при достижении определенного критического значения энергии, который приводит к изменению структуры исследуемого вещества.
Еще одним важным аспектом, которым интересуется квантовая механика в контексте плавления, является рассмотрение влияния квантовых флуктуаций. Квантовые флуктуации являются неразрывным атрибутом микрочастиц на квантовом уровне и могут быть ключевым фактором в процессе плавления, вызывая дополнительные колебания в атомах и молекулах вещества.
| В отличие от классической физики, квантовая механика предлагает новые и более глубокие объяснения процесса плавления вещества. Комплексное рассмотрение энергетических состояний и квантовых флуктуаций позволяет понять механизмы, лежащие в основе этого феномена и может привести к разработке более эффективных способов контроля плавления различных материалов. |
Влияние давления на точку плавления: влияет ли давление на превращение вещества из твёрдого состояния в жидкое?

Взаимосвязь между давлением и температурой плавления вещества относится к основным законам физики. При рассмотрении этого явления нельзя обойти вниманием роль давления, которое может оказывать дополнительное воздействие на процесс плавления.
Проявление влияния давления на точку плавления может быть объяснено особыми свойствами молекул вещества. Под действием давления межмолекулярное взаимодействие может изменяться, что приводит к изменению энергетической структуры и точки плавления вещества.
Для более подробного изучения влияния давления на точку плавления вещества были проведены различные эксперименты. Результаты этих исследований показали, что установление связи между давлением и температурой плавления вещества позволяет более точно определить условия, при которых происходит фазовый переход.
Таким образом, влияние давления на температуру плавления является важным фактором, который следует учитывать при изучении свойств вещества. Знание этой взаимосвязи позволяет более глубоко понять процессы перехода состояний вещества и применить его в различных областях науки и техники.
Теплоемкость и изменение температуры

Теплоемкость является характеристикой вещества, которая зависит от его массы и состава. Она определяет количество теплоты, необходимое для изменения температуры данного вещества на единицу массы. Изучение теплоемкости позволяет предсказывать изменения температуры и понять, как различные факторы влияют на этот процесс.
Теплоемкость может быть выражена количеством теплоты, необходимым для нагрева или охлаждения единицы массы вещества на определенное количество градусов. Это включает в себя понятие удельной теплоемкости, которая выражает количество тепла, необходимое для изменения температуры единицы массы вещества.
Понимание влияния теплоемкости на изменение температуры вещества является важной основой для изучения теплопередачи, превращений фаз и других процессов, связанных с изменением состояния вещества под воздействием тепла. Теплоемкость также оказывает влияние на процессы, связанные с нагреванием и охлаждением различных материалов, что имеет практическое применение в нашей повседневной жизни.
| Факторы, влияющие на теплоемкость |
|---|
| 1. Состав вещества |
| 2. Масса вещества |
| 3. Температура изменения |
| 4. Присутствие примесей |
| 5. Давление |
Учет различных факторов, влияющих на теплоемкость, является важной задачей при проведении тепловых расчетов и проектировании различных систем и устройств, включая тепловые двигатели, системы отопления и охлаждения, а также процессы в промышленных установках.
Вещества с разной теплоемкостью при смене фазы агрегациии

Вещества с малой теплоемкостью во время плавления обычно достигают фазовой переходной точки быстрее и с меньшими энергетическими затратами. Однако, затраты энергии также зависят от массы и структуры вещества, что может сказываться на объеме расходов энергии при смене фазы.
В противоположность веществам с малой теплоемкостью, вещества с большой теплоемкостью могут требовать более длительного времени для достижения фазовой переходной точки, а также более значительных энергетических затрат. Это связано с необходимостью накопления достаточного количества теплоты для преодоления сил притяжения между молекулами вещества.
- Вещества с низкой теплоемкостью могут менять свою фазу агрегации быстрее и с меньшим количеством энергии.
- Вещества с высокой теплоемкостью требуют более длительного времени и больше энергии для смены фазы агрегации.
Изучение и понимание различной теплоемкости различных веществ при плавлении является важным фактором при проведении экспериментов и разработке процессов, связанных с изменением температуры и сменой фазы агрегации. Это также позволяет более эффективно контролировать и использовать тепловую энергию в промышленности и научных исследованиях.
Терморегуляция взаимного теплообмена при изменении температуры
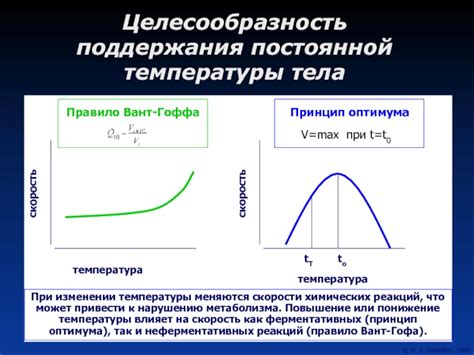
Данный раздел посвящен изучению феномена теплообмена между объектами при изменении их температуры. Учет этого эффекта необходим для понимания процессов теплопроводности и термодинамики в различных системах.
Механизм теплообмена основан на передаче тепла между объектами, когда они находятся при различных температурах. При этом происходит движение энергии от объекта с более высокой температурой к объекту с более низкой. Этот феномен возникает из-за разницы во внутренней энергии молекул, которая изменяется при изменении температуры.
Терморегуляция является ключевым аспектом теплообмена, так как она позволяет контролировать количество передаваемого тепла. Она может быть регулирована различными факторами, такими как поверхность объекта, его состав, окружающая среда и т. д. Эффект теплообмена при изменении температуры может привести как к нагреванию, так и охлаждению объектов в зависимости от этих факторов.
Детальное понимание эффекта теплообмена при изменении температуры является необходимым для разработки эффективных систем охлаждения и нагрева, а также для изучения поведения различных материалов при воздействии тепла.
Вопрос-ответ

Каким образом происходит плавление тела?
Плавление тела происходит при достижении определенной температуры, называемой температурой плавления. В этот момент межмолекулярные силы преодолеваются, и твердое вещество переходит в жидкое состояние. При повышении температуры жидкость становится все более подвижной и ее молекулы начинают перемещаться в разных направлениях.
Какие факторы влияют на температуру плавления тела?
На температуру плавления тела влияют несколько факторов. Один из них - химический состав вещества. Разные вещества имеют разные температуры плавления из-за различного взаимодействия их молекул. Также важны внешние условия, например атмосферное давление и наличие примесей. Давление может повышать или понижать температуру плавления, а примеси могут сдвигать ее в одну или другую сторону.
Что такое удельная теплота плавления?
Удельная теплота плавления - это количество теплоты, которое необходимо подать или отнять от единицы массы вещества, чтобы пройти фазовый переход из твердого состояния в жидкое при постоянной температуре. Обычно удельная теплота плавления выражается в джоулях на грамм или калориях на грамм. Этот параметр является характеристикой каждого конкретного вещества.
Какие законы относятся к изменению температуры при плавлении тела?
Одним из основных законов, связанных с плавлением тела, является закон Гейзера-Майкла. Он гласит, что количество подведенного или отнятого тепла, необходимого для изменения температуры вещества при плавлении, пропорционально массе вещества и его удельной теплоте плавления. Также есть закон Гейзера-Шлоттера, который устанавливает зависимость между температурой плавления и давлением.



