Когда мы говорим о веществах, которые находятся подле друг друга, мы редко задумываемся о замысловатых химических процессах, происходящих между ними. В современной науке много таких комбинаций, которые стали источником удивления и исследования для химиков всего мира. Одной из таких загадочных пар является оксид алюминия и соляная кислота.
Зачастую в мире химических элементов на первый взгляд самые обычные и незаметные соединения могут стать объектами научного интереса. Казалось бы, что может быть интересного в взаимодействии простейших химических элементов, не имеющих ничего зрелищного или притягательного? Ответ кроется в их потенциальной реакционной способности и тех изменениях, которые они могут вызвать друг в друге.
Соединение оксида алюминия с соляной кислотой - самобытным химическим танцем, в котором каждая молекула вещества исполняет свою уникальную роль. Здесь можно встретить жгучие искорки беспощадной реакции, так же как и нежные нотки и колебания, пронизывающие все пространство смеси. Идеальное сочетание двух совершенно разных элементов позволяет представить новое измерение соединений, полное неожиданных переливов и эффектов.
Химические свойства алюминиевого оксида

Данный раздел посвящен изучению химических свойств алюминиевого оксида, нерастворимого соединения, образующегося при взаимодействии алюминия с кислородом.
Одно из основных свойств алюминиевого оксида – его инертность. Он не образует ионов в водных растворах и обладает нейтральной реакцией. Вследствие этого, алюминиевый оксид часто используется в различных областях, где требуется устойчивость к воздействию кислот и щелочей.
Кроме того, алюминиевый оксид является термически стабильным соединением, что позволяет использовать его в качестве защитного покрытия для алюминиевых поверхностей, обеспечивая им долговечность и стойкость к окислению.
Важной химической особенностью алюминиевого оксида является его способность образовывать сложные соединения с различными кислотами и основаниями. Это свойство позволяет алюминиевому оксиду служить сырьем для получения многих важных химических соединений, используемых в промышленности и научных исследованиях.
Структура и содержание алуминатного соединения
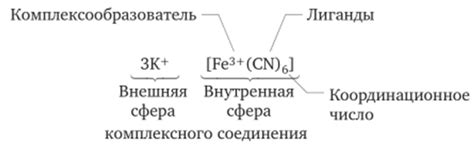
В данном разделе мы рассмотрим структуру и состав соединения, получаемого путем взаимодействия схематически представленных коагуляторов. Основной акцент будет сделан на области структурной химии и молекулярной геометрии такого важного вещества, как оксид алюминия.
В связи с большим вариантном строением алуминатных соединений, состоящих из атомов алюминия и кислорода, можно выделить несколько основных кристаллографических структур. Различия в структуре воздействуют на свойства и реакционную способность оксида алюминия. Именно поэтому его способность к растворению в соляной кислоте является объектом интереса для множества исследователей.
| Структура | Описание |
|---|---|
| Аморфный оксид алюминия | Не имеет закономерного строения, представлен в виде нерегулярно расположенных частиц, обладает большой поверхностью и хорошими адсорбционными свойствами. |
| Гибкое строение | Состоит из графитного листа, на котором атомы алюминия и кислорода занимают определенные позиции. Обладает механической гибкостью и служит основой для синтеза различных структурных модификаций. |
| Гидратированная структура | Представляет собой геометрически проложенные каналы, в которых находятся молекулы воды. Обладает высокой площадью поверхности, что обуславливает ее хорошие каталитические свойства. |
Таким образом, структура и состав оксида алюминия являются ключевыми факторами, влияющими на его химические и физические свойства. Комплексное изучение этих параметров позволяет более глубоко понять взаимодействие оксида алюминия с соляной кислотой и его роль в различных химических реакциях.
Физические свойства оксида алюминия

В данном разделе рассматриваются физические свойства соединения алюминия с кислородом, известного также как оксид алюминия. Обратим внимание на общую идею этих свойств, не используя конкретных определений или терминов.
Оксид алюминия обладает определенными характеристиками, которые определяют его поведение в различных условиях. Прежде всего, следует отметить его кристаллическую структуру, которая влияет на его физические свойства. Кроме того, оксид алюминия имеет высокую температуру плавления и кипения, что говорит о его термической устойчивости.
Одной из ключевых особенностей оксида алюминия является его твердость. Это соединение обладает высокой твердостью, что делает его прочным и устойчивым к механическим воздействиям. Кроме того, он обладает низкой проводимостью тепла и электричества, что может быть полезным в различных приложениях. Важно отметить также его относительно невысокую плотность, что делает оксид алюминия легким материалом при использовании в технике и строительстве.
Оксид алюминия имеет также высокую устойчивость к химическим воздействиям, что делает его стойким в различных средах. Он не растворяется в воде или в щелочных растворах, но может реагировать с кислотами в зависимости от их концентрации и условий.
Таким образом, физические свойства оксида алюминия определяют его уникальные характеристики и полезность в различных областях применения. Изучение этих свойств помогает лучше понять его поведение и использовать его в наиболее эффективном и безопасном образе.
| Твердость | Температура плавления и кипения | Проводимость тепла и электричества | Плотность | Химическая устойчивость |
|---|---|---|---|---|
| Высокая | Высокая | Низкая | Относительно невысокая | Высокая |
Химические свойства соляной кислоты

В данном разделе мы будем изучать особенности взаимодействия вещества, которое можно охарактеризовать как сильную кислоту, плавающую в воздухе и впитывающую в себя влагу из окружающей среды.
Точка хрупкости: Кислота, имеющая сильные химические свойства, способна протащиться сквозь множество материалов, даже основанных на алюминии и оксиде. Ее реактивность может вызывать проблемы при обращении с ней: достаточно небольшого количества этой кислоты, чтобы она превратилась в опасное вещество.
Взаимодействие с водой: Соляная кислота обладает уникальным свойством растворяться в воде со значительным выделением тепла. При этом она способна представлять опасность для человека и окружающей среды, так как встречает препятствия на своем пути, не только расщепляет, но и нагревает воду.
Окислительные свойства: Соляная кислота проявляет активные окислительные свойства при взаимодействии с рядом других веществ. Она способна изменять свою окраску и форму, вызывая протекание химической реакции.
Используйте осторожность и принимайте необходимые меры безопасности при обращении с соляной кислотой, чтобы избежать нежелательных последствий и обеспечить безопасность окружающей среды.
Взаимодействие металлов с компонентами оксида алюминия и соляной кислоты
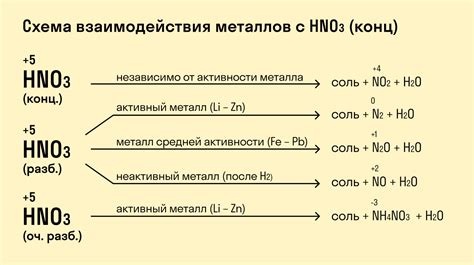
Одним из типичных взаимодействий является нейтрализационная реакция между металлом и соляной кислотой. При этом, активные металлы, такие как магний, алюминий или цинк, реагируют с кислотой, образуя соли и выделяя молекулы водорода. Реакционная способность металлов в данном случае может быть определена их электрохимическим потенциалом.
Реакция металлов с компонентами оксида алюминия также имеет место. Однако, в отличие от нейтрализации с соляной кислотой, здесь происходит окислительно-восстановительное взаимодействие. Некоторые металлы, например, железо или никель, обладают способностью к реакции с оксидами алюминия, приводя к образованию металлического алюминия и оксида металла. Такие реакции могут протекать только при определенных температурных условиях и требуют специальной обработки материалов.
- Описанные реакции имеют широкие практические приложения в различных областях науки и промышленности.
- Понимание процессов, происходящих при взаимодействии металлов с оксидом алюминия и соляной кислотой, позволяет разрабатывать новые материалы и технологии с определенными свойствами и возможностями.
- Данные реакции также могут быть использованы для синтеза различных веществ, применяемых в химической промышленности.
В итоге, изучение реакций между металлами и компонентами оксида алюминия и соляной кислоты является актуальным и интересным направлением химических исследований, которое имеет большой потенциал для применения в разных областях науки и промышленности.
Взаимодействие с основаниями

Нейтрализация
Когда оксид алюминия и соляная кислота вступают в реакцию с основаниями, происходит процесс нейтрализации. В результате этой реакции образуются соли и вода. Вода при этом является одним из продуктов реакции и обладает сильными химическими свойствами. Нейтрализация с основаниями позволяет смягчить их кислотные свойства и привести к образованию новых соединений с другими физическими и химическими свойствами.
Образование алюминиевых солей
При взаимодействии оксида алюминия и соляной кислоты с основаниями образуются алюминиевые соли. Эти соединения обладают различными свойствами и могут применяться в различных областях науки и промышленности. Алюминиевые соли часто используются в качестве катализаторов, добавок в лекарственные препараты и производстве красителей и пигментов.
Роль оснований в реакции
Основания играют важную роль в реакции между оксидом алюминия и соляной кислотой. Они не только участвуют в химической реакции и образовании новых соединений, но и оказывают влияние на скорость и характер этой реакции. Также основания могут использоваться для регулирования pH-уровня в реакционной среде и обеспечения оптимальных условий для протекания химической реакции.
Взаимодействие с карбонатами и гидроксидами

В данном разделе рассмотрим взаимодействие оксида алюминия с различными соединениями, такими как карбонаты и гидроксиды.
Карбонаты представляют собой соли угольной кислоты, содержащие карбонат-ион (КО3^2-) и металлический ион. Они обладают щелочными свойствами и могут реагировать с оксидами алюминия, приводя к образованию солей и выделению углекислого газа (СО2). Это взаимодействие может происходить в водных растворах или в твердом состоянии, при нагревании.
Гидроксиды представляют собой соединения, в которых металл замещает один из атомов в гидроксильной группе (ОН-). Они имеют щелочные свойства и также могут реагировать с оксидами алюминия, образуя соли и воду. Реакция может протекать в водных растворах или при сухом взаимодействии.
| Тип соединения | Реакция с оксидом алюминия |
|---|---|
| Карбонаты | Оксид алюминия + карбонат → соль + углекислый газ |
| Гидроксиды | Оксид алюминия + гидроксид → соль + вода |
Таким образом, взаимодействие оксида алюминия с карбонатами и гидроксидами приводит к образованию новых соединений и может сопровождаться выделением газов или воды. Эти реакции являются важными для понимания процессов, связанных с оксидом алюминия в различных системах и условиях среды.
Взаимодействие амфотерного оксида с кислотой

Взаимодействие амфотерного оксида с кислотой является типичным примером химической реакции, в результате которой образуются соли и вода. При этом происходит передача протонов между веществами, что приводит к изменению их свойств и образованию новых соединений.
В зависимости от конкретных условий, взаимодействие амфотерного оксида с кислотой может проявляться как образование кислотных солей, так и основных солей. Это зависит от химической природы оксида и его способности принимать или отдавать протоны в процессе реакции.
Взаимодействие амфотерного оксида с кислотой является важным процессом в химии и находит применение в различных областях, включая промышленность и научные исследования. Точное понимание этой реакции позволяет предсказывать ее результаты и контролировать химические процессы.
Механизм и условия протекания химической превращения

Данный раздел посвящен изучению механизма и определению условий, при которых происходит химическое взаимодействие между субстанциями, представленными не имеющими отношения к оксиду алюминия и соляной кислоте, но включающими аналогичные химические процессы.
- Роли исходных компонентов. Анализ влияния физико-химических свойств исходных компонентов на ход реакции.
- Стадии протекания реакции. Рассмотрение последовательности этапов, начиная от инициирующей стадии до образования конечных продуктов.
- Энергетика реакции. Исследование энергетических параметров, таких как активационная энергия и энтальпия, для оценки стабильности и скорости протекания реакции.
- Кинетические модели. Описание различных кинетических моделей, позволяющих описать зависимость скорости реакции от концентраций реагентов и температуры.
В этом разделе также будут рассмотрены факторы, влияющие на протекание химической реакции, такие как температура, концентрация реагентов, pH-уровень, наличие катализаторов и т.д. Подробное изучение этих условий позволит нам понять, какие факторы могут ускорить или замедлить химическую превращение, а также определить оптимальные условия для получения желаемых продуктов.
Вопрос-ответ

Каким образом происходит взаимодействие оксида алюминия и соляной кислоты?
Взаимодействие оксида алюминия (Al2O3) и соляной кислоты (HCl) приводит к образованию соли алюминия хлорида (AlCl3) и воды (H2O). По сути, оксид алюминия реагирует с соляной кислотой, образуя хлорид алюминия и воду.
Какие химические реакции происходят при взаимодействии оксида алюминия и соляной кислоты?
Взаимодействие оксида алюминия и соляной кислоты приводит к осуществлению ряда химических реакций, которые заключаются в образовании хлорида алюминия (AlCl3) и воды (H2O). Эта реакция можно описать следующим образом: Al2O3 + 6HCl = 2AlCl3 + 3H2O.
Какое значение имеет реакция между оксидом алюминия и соляной кислотой с практической точки зрения?
Реакция между оксидом алюминия и соляной кислотой является важной с практической точки зрения, так как позволяет получать хлорид алюминия (AlCl3), который находит применение в различных отраслях промышленности. Хлорид алюминия используется как катализатор в органическом синтезе, в процессе получения полимеров и каучука, а также в производстве лекарственных средств и косметических продуктов.
Почему исследование реакции между оксидом алюминия и соляной кислотой важно для науки?
Исследование реакции между оксидом алюминия и соляной кислотой имеет важное значение для науки, так как позволяет более глубоко изучить химические свойства данных веществ и их взаимодействие. Это помогает расширить наши знания о принципах химии и использовать эти знания в различных областях, включая промышленность, медицину, косметологию и другие.
Можно ли использовать оксид алюминия и соляную кислоту для образования других химических соединений?
Да, оксид алюминия и соляная кислота могут быть использованы для образования других химических соединений. Например, путем взаимодействия оксида алюминия с соляной кислотой можно получить хлорид алюминия (AlCl3), а также образующуюся в результате воду (H2O) можно использовать для других химических реакций.
Какие реакции могут происходить между оксидом алюминия и соляной кислотой?
Между оксидом алюминия (Al2O3) и соляной кислотой (HCl) может происходить реакция образования алюминия хлорида (AlCl3) и воды (H2O). Формула этой реакции может быть записана следующим образом: Al2O3 + 6HCl → 2AlCl3 + 3H2O. Это реакция обмена, в результате которой происходит образование новых веществ.



