Одно из важнейших и научно значимых уравнений, изучаемых в области химии и термодинамики, уравнение Менделеева-Клапейрона, открывает перед нами мир бесконечных возможностей и закономерностей. Погрузившись в эту область, мы сталкиваемся с разнообразием переменных и компонентов, влияющих на химическую реакцию. И тут на сцену выходит буква r, которая играет редуктивную роль, придающую уравнению Менделеева-Клапейрона глубокий смысл и объединяющую множество ключевых факторов.
Загадка r не раскрывает своего значения сразу же, а требует внимательного и осторожного анализа в контексте уравнения Менделеева-Клапейрона и его применения в реальном мире. Она воплощает в себе всеобъемлющую силу притяжения, тесно связанную с данным уравнением, исследуя пространство и взаимодействие молекул вещества.
В своей глубине r является ответом на вопросы о возможностях химической реакции и распределении энергии в системе. Именно r дает нам ключ к пониманию степени возможной концентрации вещества и его влияния на реакционную среду. За r кроется также и понимание границы, определяющей фазовую диаграмму и переходы между состояниями вещества в химическом процессе.
Что скрывается за уравнением Менделеева-Клапейрона
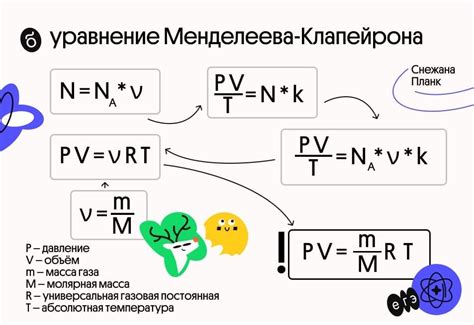
Эта часть статьи посвящена пониманию сущности уравнения Менделеева-Клапейрона и его важности в физико-химических расчетах. Однако прежде чем мы углубимся в детали, давайте рассмотрим его с общей точки зрения. Уравнение Менделеева-Клапейрона представляет собой мощный инструмент, который позволяет связать несколько фундаментальных свойств вещества и использовать их для вычисления других параметров.
Это уравнение может быть рассмотрено как своего рода закон сохранения, который объединяет такие важные величины, как давление, температура, объем и количество вещества в рамках одного математического выражения. Оно является ключевым инструментом в области химической термодинамики и является основой для множества расчетов и прогнозов, связанных с физико-химическими процессами.
- Оно позволяет определить отношения между различными энергетическими состояниями вещества при изменении условий эксперимента.
- Оно используется для расчета количественных параметров, таких как работа, тепловой эффект, изменение энтропии и энтальпии.
- Оно имеет широкое применение в различных областях, включая физику, химию, материаловедение и металлургию.
Итак, уравнение Менделеева-Клапейрона является не просто формулой, но концептуальным инструментом, который позволяет нам увидеть и понять взаимосвязи между различными физико-химическими свойствами вещества. В следующих разделах мы рассмотрим его математическую форму и применение на примерах, чтобы полностью освоить эту концепцию и использовать ее в нашей работе.
Основная цель и суть уравнения Менделеева-Клапейрона

- Главной целью уравнения Менделеева-Клапейрона является описание математической зависимости между различными физическими величинами, определяющими состояние газового образца. Уравнение позволяет предсказать поведение и свойства газа при изменении условий с помощью простой и удобной формулы.
- Описывая поведение и свойства газов, уравнение Менделеева-Клапейрона позволяет установить закономерности в изменении этих параметров при изменении других величин, таких как температура, давление или объем. Таким образом, оно способствует пониманию и изучению физических и химических процессов, связанных с газами.
- Более того, уравнение Менделеева-Клапейрона является основополагающим законом в области физико-химических расчетов. Оно находит применение в различных областях науки и техники, таких как термодинамика, химическая кинетика, газовая хроматография и другие.
- Вычисления, произведенные с использованием уравнения Менделеева-Клапейрона, позволяют предсказать изменения параметров газа при различных условиях и определить оптимальные условия для различных процессов, связанных с газами, как в лабораторных, так и в промышленных условиях.
- Таким образом, уравнение Менделеева-Клапейрона является важным инструментом для научного и инженерного прогресса, обеспечивая понимание и контроль над физико-химическими процессами, связанными с газами.
Применение уравнения Менделеева-Клапейрона в химии

Применяя уравнение Менделеева-Клапейрона, исследователи могут определить такие параметры, как давление, объем, температура и количество вещества газов. Это позволяет им проводить качественный анализ положения равновесия в химических реакциях, а также предсказывать кинетические и термодинамические свойства веществ.
Приведу несколько примеров применения уравнения Менделеева-Клапейрона в химии:
| Пример | Описание |
|---|---|
| Вычисление молярной массы газа | Уравнение позволяет определить массу молекул газа по его давлению, объему и температуре. |
| Определение плотности газовой смеси | Уравнение позволяет вычислить плотность смеси газов по их давлению, температуре и молярной массе. |
| Расчет концентрации вещества в газовой смеси | Уравнение позволяет определить количество вещества в смеси газов по их давлению, температуре и объему. |
| Оценка равновесного состояния реакции | Уравнение позволяет вычислить константу равновесия и определить, в какой степени реакция протекает в направлении образования продуктов или реагентов. |
Это лишь некоторые из множества возможностей, открываемых уравнением Менделеева-Клапейрона, которые имеют огромное значение для изучения химических процессов и развития химической науки в целом.
Роль универсальной газовой постоянной в уравнении Менделеева-Клапейрона
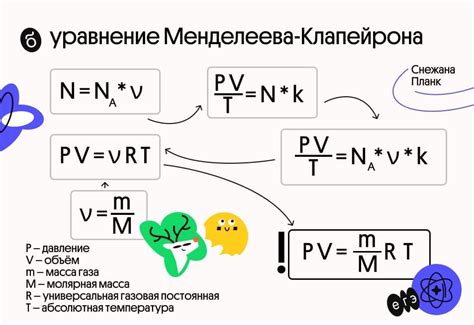
Универсальная газовая постоянная - это фундаментальная константа, которая связывает макроскопические величины, такие как давление, температура и объем, с молекулярными характеристиками газов. Она является своеобразным коэффициентом масштабирования, позволяющим перейти от молекулярных величин к макроскопическим и наоборот.
Универсальная газовая постоянная выражает непосредственную связь между физическими параметрами газов и их структурой на молекулярном уровне. Она определяется через соотношение между количеством вещества, называемым молярным количеством, а также другими физическими константами, такими как число Авогадро и универсальная газовая постоянная Больцмана.
Значение универсальной газовой постоянной в уравнении Менделеева-Клапейрона позволяет не только определить количество вещества газа при известных значениях давления, объема и температуры, но и связать между собой термодинамические и кинетические свойства газов. Оно также позволяет проводить сравнение и анализ различных газовых систем в условиях изменения параметров и предсказывать их поведение при изменении внешних условий.
Роль универсальной газовой постоянной в уравнении Менделеева-Клапейрона

Универсальная газовая постоянная, обозначаемая как r или R, является физической константой и имеет одинаковое значение для всех газов при стандартных условиях. Она представляет собой связь между физическими свойствами газа и его молекулярной структурой. В уравнении Менделеева-Клапейрона универсальная газовая постоянная служит масштабирующим коэффициентом, позволяющим перевести единицы измерения давления, объема и температуры в удобные для работы значения.
Применение универсальной газовой постоянной в уравнении Менделеева-Клапейрона позволяет рассчитывать различные параметры газовой системы. Например, она может быть использована для определения количества вещества газа по известным значениям давления, объема и температуры. Также универсальная газовая постоянная позволяет сравнивать свойства различных газов и проводить сопоставление разных систем.
Из значений давления, объема и температуры можно получить информацию о молекулярной структуре газа и его физических свойствах. Универсальная газовая постоянная играет важную роль в этом процессе, обеспечивая связь между данными параметрами и характеристиками молекул газа.
Таким образом, роль универсальной газовой постоянной в уравнении Менделеева-Клапейрона заключается в обеспечении связи между физическими свойствами газа и его молекулярной структурой. Она является ключевым коэффициентом, позволяющим использовать уравнение для решения различных задач в области физической химии и газовой динамики.
Универсальная газовая постоянная и ее единицы измерения: простое объяснение

Однако сама универсальная газовая постоянная имеет определенные единицы измерения, которые необходимо учитывать при проведении различных расчетов. Единицы измерения универсальной газовой постоянной зависят от выбранных системы единиц и обычно представлены в различных форматах, таких как Па·м³/(моль·К), Дж/(моль·К) или атм·л/(моль·К).
В системе СИ универсальную газовую постоянную обычно обозначают символом R и выражают в Па·м³/(моль·К), где Па обозначает паскаль, м³ - кубический метр, моль - количество вещества, а К - кельвин, шкала, используемая для измерения температуры.
Отметим, что единицы измерения универсальной газовой постоянной должны соответствовать использованной системе единиц всех остальных параметров в задаче, чтобы обеспечить согласованность результатов расчетов. Поэтому при работе с уравнением Менделеева-Клапейрона и решении задач на газы важно правильно подбирать и использовать единицы измерения универсальной газовой постоянной.
Как применять уравнение Менделеева-Клапейрона для решения задач
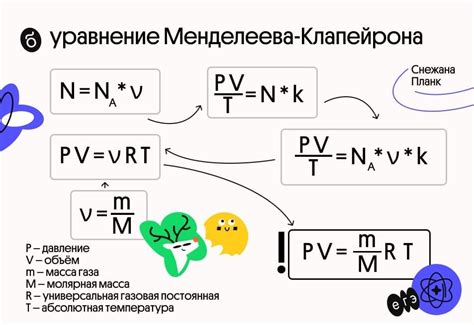
Применение уравнения Менделеева-Клапейрона может быть весьма широким и полезным. Например, его можно использовать для определения молярной массы вещества, расчета количества вещества, вычисления температуры и объема газа при известном давлении и т.д. Это позволяет исследователям и химикам проводить эксперименты, предсказывать результаты реакций и оптимизировать процессы в химической индустрии.
Для решения задач, связанных с уравнением Менделеева-Клапейрона, необходимо иметь некоторые начальные данные, такие как давление, объем и температуру. Затем, используя соответствующие константы и формулы, можно вычислить неизвестные параметры, например, количество вещества или молярную массу.
Примером использования уравнения Менделеева-Клапейрона может быть задача о расчете количества газа, занимающего определенный объем при определенной температуре и давлении. Зная значения этих параметров, можно применить уравнение Менделеева-Клапейрона для вычисления количества вещества газа, которое находится в системе.
Важно помнить, что для решения задач с использованием уравнения Менделеева-Клапейрона необходимо учитывать единицы измерения и использовать соответствующие константы величин. Также стоит учесть, что данное уравнение предполагает идеальное поведение газа и не применимо к реальным системам, где могут иметь место такие явления, как силы притяжения или отталкивания между молекулами.
Шаги при решении задач на основе уравнения Менделеева-Клапейрона

Эффективное решение задач, основанных на уравнении Менделеева-Клапейрона, требует выполнения нескольких ключевых шагов.
Шаг 1: Формулировка задачи и определение известных величин.
Первым шагом в решении задачи, связанной с уравнением Менделеева-Клапейрона, необходимо четко сформулировать поставленную задачу. Затем определите все известные величины, какие данные предоставлены в условии задачи.
Шаг 2: Поиск неизвестной величины и ее обозначение.
После определения известных величин следует найти неизвестную величину, с которой необходимо работать в уравнении Менделеева-Клапейрона. Обозначьте эту величину символом или буквой для удобства дальнейших расчетов.
Шаг 3: Проверка условий задачи.
Проверьте, что все данные соответствуют условиям задачи и имеют правильные единицы измерения. Проверьте также, что данное уравнение Менделеева-Клапейрона применимо для данной задачи.
Шаг 4: Проведение необходимых преобразований уравнения Менделеева-Клапейрона.
Используя уравнение Менделеева-Клапейрона, преобразуйте его к форме, необходимой для решения поставленной задачи. Это может включать переупорядочение уравнения, замену известных величин и неизвестной величины, а также использование дополнительных уравнений и соотношений.
Шаг 5: Вычисление неизвестной величины.
После проведения всех преобразований уравнения Менделеева-Клапейрона, выполните необходимые математические операции для получения значения неизвестной величины. Ответ должен быть представлен в правильных единицах измерения и округлен до нужной точности.
Шаг 6: Проверка и интерпретация результата.
Последний шаг заключается в проверке результата с помощью логической или физической проверки. Интерпретируйте полученный результат и убедитесь, что он имеет смысл с точки зрения условия задачи и физической реальности.
Следуя этим шагам, вы сможете успешно решать задачи, основанные на уравнении Менделеева-Клапейрона, и получать корректные и смысловые результаты.
Применение уравнения Менделеева-Клапейрона в решении задач: практические примеры

В данном разделе представлены конкретные задачи, в которых применение уравнения Менделеева-Клапейрона оказывается необходимым для получения и анализа результатов. Знание и понимание этого уравнения является важным инструментом для химиков, физиков и специалистов в смежных областях.
Пример 1:
Представим ситуацию, где требуется расчет количества газа в реакционной смеси при определенных условиях. Известны объем смеси, ее температура и давление. Подставив данные в уравнение Менделеева-Клапейрона, можно определить количество вещества газа в системе и провести дальнейшие расчеты, необходимые для анализа реакций и процессов.
Пример 2:
Рассмотрим задачу, где требуется вычислить объем газа, зная температуру, количество вещества и давление. Благодаря уравнению Менделеева-Клапейрона, можно легко определить нужное значение и получить необходимые результаты для продолжения исследования или практических расчетов.
Через примеры решения задач с применением уравнения Менделеева-Клапейрона становится ясно, что это важная концепция в химических и физических науках. Понимание и умение применять это уравнение позволят исследователям и специалистам вносить новые открытия и расширять границы научного знания.
Вопрос-ответ

Какое значение имеет r в уравнении Менделеева-Клапейрона?
Значение r в уравнении Менделеева-Клапейрона представляет газовую постоянную. Его численное значение равно 8,314 Дж/(моль·К).
Почему значение r в уравнении Менделеева-Клапейрона так важно?
Значение r в уравнении Менделеева-Клапейрона является важным, поскольку оно связано с физическими свойствами газов и позволяет проводить расчеты, связанные с их объемом, давлением, температурой и количеством вещества.
Каково значение r в уравнении Менделеева-Клапейрона в СИ?
Значение r в уравнении Менделеева-Клапейрона в СИ равно 8,314 Дж/(моль·К).
Можно ли использовать уравнение Менделеева-Клапейрона без газовой постоянной r?
Нет, уравнение Менделеева-Клапейрона нельзя использовать без газовой постоянной r, поскольку оно основано на этой константе. Она необходима для проведения расчетов и связи между физическими свойствами газов.
Какими примерами можно проиллюстрировать применение уравнения Менделеева-Клапейрона с газовой постоянной r?
Один из примеров применения уравнения Менделеева-Клапейрона с газовой постоянной r может быть расчет условий идеального газа, например, определение его объема при заданной температуре и давлении. Также, уравнение может быть использовано для расчета количества вещества газа или изменения его давления при изменении других параметров.
Какое значение имеет r в уравнении Менделеева-Клапейрона?
Значение r в уравнении Менделеева-Клапейрона обозначает универсальную газовую постоянную. В обычной международной системе единиц оно равно примерно 8,314 Дж/(моль·К).



